La pericarditis constrictiva (PC) es una forma relativamente infrecuente de insuficiencia cardiaca clínica. Se desconoce la verdadera prevalencia en la población, pero se ha estimado que entre las personas con pericarditis vírica se produce en menos del 0,5% de los casos.1 Sin embargo, dado que es potencialmente reversible, el diagnóstico no debe pasarse por alto. La pericardiectomía quirúrgica tiene la capacidad de «curar» la PC, con una mejora espectacular de los síntomas y la calidad de vida.2,3 Aunque la etiología de la PC puede ser variada (idiopática, postvírica, tuberculosa, postquirúrgica, inducida por la radiación, etc.), la vía común final es el desarrollo de un engrosamiento fibroso o una calcificación del pericardio que da lugar a la no conformidad pericárdica.
Fisiología y fisiopatología pericárdica en la constricción:
El pericardio normal impide mínimamente la distensibilidad ventricular en volúmenes operativos cardíacos normales. En la PC, la falta de conformidad del pericardio crea una unidad ventrículo-pericardio rígida, lo que conduce a un aumento de las presiones diastólicas y a un incremento más rápido de las presiones ventriculares para un retorno venoso determinado. El pericardio no conforme limita la relajación ventricular y determina la presión diastólica ventricular, lo que da lugar a presiones diastólicas elevadas e igualadas en todas las cámaras. Clínicamente, esto se presenta predominantemente como congestión del lado derecho (distensión venosa yugular, edema y ascitis). La elevación de la presión capilar pulmonar en cuña y la disminución de la respuesta del gasto cardíaco al ejercicio (dado un llenado ventricular inadecuado) dan lugar a disnea e intolerancia al esfuerzo, aunque el edema pulmonar franco es menos frecuente que la insuficiencia cardíaca sistólica típica.
El pericardio normal regula el acoplamiento de los volúmenes sistémicos del lado izquierdo y derecho durante los cambios agudos en la precarga, de manera que un aumento repentino del retorno venoso del lado derecho (durante la inspiración) se asocia con un arqueamiento septal hacia la izquierda y una disminución de la presión de llenado transmural del ventrículo izquierdo (presión pericárdica de la presión diastólica del VI). Esto, a su vez, disminuye el volumen diastólico final del VI (precarga del VI) y, por tanto, el volumen sistólico del lado izquierdo.4 En el corazón normal, estos cambios en el volumen sistólico con la respiración son mínimos. Dado un volumen pericárdico fijo en la PC, el acoplamiento pericárdico es muy exagerado, lo que lleva a una dramática interdependencia ventricular. El movimiento septal ventricular anormal es el resultado de las alteraciones respirofásicas aumentadas en el volumen sistólico izquierdo y derecho.
En la PC, debido a que el corazón está envuelto por un pericardio no flexible, la disminución inspiratoria normal de la presión intratorácica no se transmite a las presiones intracardíacas. Este efecto amplifica los descensos inspiratorios de la presión venosa pulmonar (ya que las venas pulmonares son principalmente extrapericárdicas), lo que se traduce en una reducción de la precarga inspiratoria del lado izquierdo, reduciendo aún más el volumen sistólico inspiratorio del lado izquierdo. La evaluación diagnóstica multimodal de la PC pone de manifiesto estos hallazgos, facilitando el diagnóstico.
Evaluación inicial:
La baja prevalencia de la PC hace que la identificación de las características clave de la exploración física y de los antecedentes sea un paso inicial importante en el proceso diagnóstico. Los antecedentes de cirugía cardíaca, radiación o tuberculosis deben aumentar la sospecha clínica en presencia de edema, distensión abdominal y disnea de esfuerzo. La presión venosa yugular (PVJ) elevada está presente en prácticamente todos los pacientes que no son hipovolémicos. La restricción pericárdica provoca la incapacidad del corazón derecho para acomodar el retorno venoso abdominal inspiratorio, lo que se traduce en un aumento inspiratorio de la PVC (signo de Kussmaul).5 Los descensos yugulares en x e y son prominentes en la PC, debido al movimiento anular longitudinal exagerado y al llenado ventricular temprano prominente, respectivamente. Por el contrario, la miocardiopatía restrictiva muestra un embotamiento del descenso en x, debido a un deterioro de la relajación auricular y a una miopatía auricular. La auscultación puede revelar un golpe pericárdico agudo a lo largo del borde esternal izquierdo. La ascitis y el edema inferior significativo son comunes y a menudo conducen a un diagnóstico erróneo de enfermedad hepática si no se reconocen los hallazgos del JVP.
Las pruebas de laboratorio en la PC son inespecíficas. Un BNP elevado puede sugerir una mayor probabilidad de miocardiopatía restrictiva, pero los estudios han mostrado un gran solapamiento en los valores diagnósticos en esta población, lo que limita la utilidad clínica.6-9
Ecocardiografía:
Como prueba diagnóstica inicial, la ecocardiografía puede confirmar el diagnóstico de PC en la mayoría de los casos si la probabilidad previa a la prueba es suficientemente alta.10 La ecocardiografía demuestra características tanto de interdependencia ventricular exagerada como de disociación intratorácica-intracardíaca. El hallazgo patognomónico es el desplazamiento septal respirofásico, detectado tanto por el modo M como por las imágenes 2D.5 Además de este movimiento septal respiratorio exagerado, también hay un movimiento septal anormal entre latidos, o «temblor», debido al llenado diastólico rápido diferencial del ventrículo derecho y luego del izquierdo.11 La vena cava inferior es universalmente pletórica en ausencia de hipovolemia; una característica sensible pero no específica de la PC. Las inversiones espiratorias de la vena hepática y la disminución del flujo diastólico hacia delante se producen debido al movimiento septal ventricular hacia la derecha por un aumento espiratorio de la precarga del VI, con la consiguiente disminución de la distensibilidad efectiva del ventrículo derecho.
Los cambios exagerados de la precarga respiratoria también se ejemplifican con una disminución inspiratoria del Doppler de entrada de la válvula mitral y un aumento del Doppler de entrada de la válvula tricúspide. Sin embargo, estos hallazgos son insensibles. En presencia de presiones de cuña capilar pulmonar y auricular izquierda significativamente aumentadas, la disminución del gradiente de presión de cuña-LV con la inspiración es insuficiente para cambiar la precarga del VI lo suficiente como para alterar la magnitud del Doppler de entrada mitral.12 Debido a la sujeción de la pared lateral, la velocidad Doppler tisular diastólica temprana (e’) del anillo mitral lateral suele estar disminuida y ser anormalmente más baja que la velocidad e’ medial (annulus reversus).13 A diferencia de las causas cardiomiopáticas de la insuficiencia cardíaca, la velocidad e’ medial es relativamente normal (o incluso está aumentada, lo que se denomina annulus paradoxus) dada la relajación miocárdica normal y el movimiento longitudinal anular medial compensatorio en el contexto de la sujeción de la pared lateral.14,15
Radiología cardiaca:
En la PC, las radiografías de tórax pueden demostrar calcificación pericárdica, un hallazgo patognomónico en presencia de insuficiencia cardiaca clínica y elevación de la VJ. La TC de tórax es más sensible a la calcificación pericárdica que la radiografía de tórax.16 La TC de tórax y la RM permiten medir con precisión el grosor del pericardio, y la RM, en particular, ha demostrado una excelente precisión (93%) en la detección de un engrosamiento pericárdico >4 mm.17 Sin embargo, es importante recordar que hasta el 18% de los casos de PC confirmada quirúrgicamente pueden tener un grosor pericárdico normal a pesar del incumplimiento patológico.18 El anclaje pericárdico, que puede visualizarse mediante ecocardiografía, TC o RM, también puede proporcionar información sobre la presencia de PC. La RM aporta información sobre la inflamación pericárdica activa, que puede ayudar a orientar las decisiones terapéuticas. Además, la IRM cardíaca proporciona una evaluación única del miocardio, que puede identificar procesos cardiomiopáticos cuando el diagnóstico es incierto. El realce tardío del miocardio suele estar ausente en la PC aislada, pero puede darse en casi un tercio de los casos con miocardiopatía restrictiva.19
A diferencia de la ecocardiografía, la TC y la RM cardíacas no dependen del hábito del paciente y pueden proporcionar una mejor visualización cardíaca cuando las imágenes ecocardiográficas no son óptimas. Los desplazamientos respirofásicos en el movimiento septal están bien demostrados tanto en la TC como en la RM. Además, la TC y la RM pueden proporcionar información sobre causas alternativas de disnea, como enfermedades pulmonares o parálisis diafragmática.
Diagnóstico más allá de las imágenes cardíacas:
El cateterismo cardíaco sigue siendo la prueba diagnóstica de referencia, si las pruebas no invasivas no son concluyentes, para valorar la presencia de constricción y evaluar la importancia hemodinámica. Aunque la mayoría de los pacientes con PC no requieren un cateterismo hemodinámico para el diagnóstico, un subgrupo de especial interés es el de los pacientes con cardiopatía por radiación, en los que a menudo es difícil identificar el grado de miocardiopatía restrictiva subyacente, incluso si hay rasgos constrictivos. Incluso con una ecocardiografía y una radiología cardíaca de alta calidad, estos pacientes pueden requerir un cateterismo hemodinámico invasivo para evaluar la elevación de las presiones de llenado con igualación diastólica, la interdependencia ventricular y la disociación intratorácica-intracardíaca.2
Tratamiento:
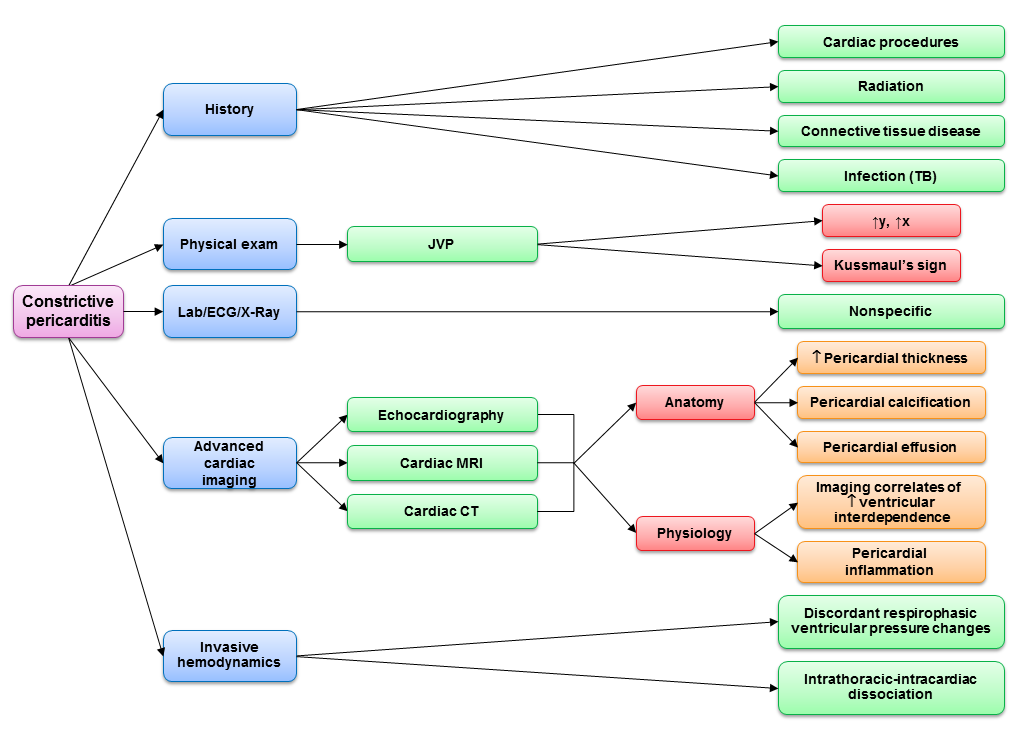
Una vez identificada la PC, el tratamiento médico con diuresis suele ser sólo parcialmente eficaz para paliar los síntomas. Si hay una inflamación pericárdica extensa, se justifica un ensayo de tratamiento antiinflamatorio para evaluar la reversibilidad antes de proceder a la pericardiectomía. Algunos pacientes pueden tener una mejora de la distensibilidad pericárdica si sólo tienen una constricción transitoria por la inflamación.20 La pericardiectomía quirúrgica completa está indicada para aliviar los síntomas en los pacientes con PC. Utilizando un enfoque diagnóstico multimodal (figura 1), actualmente es poco frecuente que los pacientes pasen por el quirófano para confirmar la PC. Dada la naturaleza a menudo transformadora de la pericardiectomía para la calidad de vida de los pacientes, los clínicos deben seguir manteniendo un alto índice de sospecha de esta forma rara pero curable de insuficiencia cardiaca.
Figura 1
- Imazio M, Brucato A, Maestroni S, et al. Riesgo de pericarditis constrictiva tras pericarditis aguda. Circulation 2011;124:1270-5.
- Geske JB, Anavekar NS, Nishimura RA, Oh JK, Gersh BJ. Diferenciación de la constricción y la restricción: hemodinámica cardiovascular compleja. J Am Coll Cardiol 2016;68:2329-47.
- Ling LH, Oh JK, Schaff HV, et al. Pericarditis constrictiva en la era moderna: evolución del espectro clínico e impacto en el resultado después de la pericardiectomía. Circulation 1999;100:1380-6.
- Kroeker CA, Shrive NG, Belenkie I, Tyberg JV. El pericardio modula los volúmenes sistémicos ventriculares izquierdo y derecho para compensar los cambios repentinos en el volumen auricular. Am J Physiol Heart Circ Physiol 2003;284:H2247-54.
- Talreja DR, Nishimura RA, Oh JK, Holmes DR. Pericarditis constrictiva en la era moderna: nuevos criterios para el diagnóstico en el laboratorio de cateterismo cardíaco. J Am Coll Cardiol 2008;51:315-9.
- Sengupta PP, Krishnamoorthy VK, Abhayaratna WP, et al. Comparación de la utilidad del Doppler tisular frente al péptido natriurético cerebral para diferenciar la enfermedad pericárdica constrictiva de la miocardiopatía restrictiva. Am J Cardiol 2008;102:357-62.
- Leya FS, Arab D, Joyal D, et al. The efficacy of brain natriuretic peptide levels in differentiating constrictive pericarditis from restrictive cardiomyopathy. J Am Coll Cardiol 2005;45:1900-2.
- Babuin L, Alegria JR, Oh JK, Nishimura RA, Jaffe AS. Brain natriuretic peptide levels in constrictive pericarditis and restrictive cardiomyopathy. J Am Coll Cardiol 2006;47:1489-91.
- Reddy PR, Dieter RS, Das P, Steen LH, Lewis BE, Leya FS. Utilidad del BNP para diferenciar la pericarditis constrictiva de la miocardiopatía restrictiva en pacientes con insuficiencia renal. J Card Fail 2007;13:668-71.
- Welch TD, Ling LH, Espinosa RE, et al. Echocardiographic diagnosis of constrictive pericarditis: Criterios de la Clínica Mayo. Circ Cardiovasc Imaging 2014;7:526-34.
- Coylewright M, Welch TD, Nishimura RA. Mecanismo del rebote septal en la pericarditis constrictiva: un estudio simultáneo de cateterismo cardíaco y ecocardiografía. Heart 2013;99:1376.
- Oh JK, Tajik AJ, Appleton CP, Hatle LK, Nishimura RA, Seward JB. Reducción de la precarga para desenmascarar los rasgos Doppler característicos de la pericarditis constrictiva: una nueva observación. Circulation 1997;95:796-9.
- Reuss CS, Wilansky SM, Lester SJ, et al. Using mitral ‘annulus reversus’ to diagnose constrictive pericarditis. Eur J Echocardiogr 2009;10:372-5.
- Ha JW, Oh JK, Ling LH, Nishimura RA, Seward JB, Tajik AJ. Annulus paradoxus: transmitral flow velocity to mitral annular velocity ratio is inversely proportional to pulmonary capillary wedge pressure in patients with constrictive pericarditis. Circulation 2001;104:976-8.
- Ha JW, Ommen SR, Tajik AJ, et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue Doppler echocardiography. Am J Cardiol 2004;94:316-9.
- Ling LH, Oh JK, Breen JF, et al. Pericarditis constrictiva calcificada: ¿sigue entre nosotros? Ann Intern Med 2000;132:444-50.
- Masui T, Finck S, Higgins CB. Constrictive pericarditis and restrictive cardiomyopathy: evaluation with MR imaging. Radiology 1992;182:369-73.
- Talreja DR, Edwards WD, Danielson GK, et al. Constrictive pericarditis in 26 patients with histologically normal pericardial thickness. Circulation 2003;108:1852-7.
- Muehlberg F, Toepper A, Fritschi S, Prothmann M, Schulz-Menger J. Aplicaciones de la resonancia magnética en las miocardiopatías infiltrativas. J Thorac Imaging 2016;31:336-47.
- Haley JH, Tajik AJ, Danielson GK, Schaff HV, Mulvagh SL, Oh JK. Pericarditis constrictiva transitoria: causas e historia natural. J Am Coll Cardiol 2004;43:271-5.
Temas clínicos: Cirugía cardíaca, Insuficiencia cardíaca y miocardiopatías, Angiografía e intervención cardiovascular invasiva, Imagen no invasiva, Enfermedad del pericardio, Cirugía cardíaca e insuficiencia cardíaca, Insuficiencia cardíaca aguda, Insuficiencia cardíaca crónica, Intervenciones e imágenes, Tomografía computarizada, Ecocardiografía/Ultrasonido, Imagen nuclear
Palabras clave: Presión arterial, Cateterismo cardíaco, Cardiomiopatía, Restrictiva, Errores de diagnóstico, Pruebas de diagnóstico, Rutina, Diuresis, Disnea, Ecocardiografía, Edema, Insuficiencia cardíaca, Sistólica, Ventrículos cardíacos, Venas hepáticas, Hipovolemia, Válvula mitral, Pericardiectomía, Pericarditis, Constrictiva, Pericardio, Edema Pulmonar, Venas Pulmonares, Presión de Cuña Pulmonar, Válvula Tricúspide, Tomografía, Rayos X Computados, Vena Cava, Inferior, Presión Venosa, Presión Ventricular, Rayos X
< Volver al listado