Konstriktiv perikardit (CP) är en relativt ovanlig form av klinisk hjärtsvikt. Den verkliga prevalensen i befolkningen är okänd, men bland dem med viral perikardit har den uppskattats förekomma i mindre än 0,5 % av fallen.1 Eftersom den är potentiellt reversibel får diagnosen dock inte missas. Kirurgisk perikardiektomi har förmågan att ”bota” CP, med dramatiska förbättringar av symtom och livskvalitet.2,3 Även om etiologin till CP kan vara varierande (idiopatisk, postviral, tuberkulös, postkirurgisk, strålningsinducerad etc.) är den sista gemensamma vägen utveckling av fibrös förtjockning eller förkalkning av perikardiet som resulterar i att perikardiet inte följer med.
Perikardiets fysiologi och patofysiologi vid konstriktion:
Det normala perikardiet hindrar minimalt den ventrikulära distensibarheten vid normala kardiella operationsvolymer. Vid CP skapar perikardiets bristande följsamhet en styv ventrikel-perikardienhet, vilket leder till ökade diastoliska tryck och snabbare ökning av ventrikeltrycken för ett givet venöst återflöde. Det icke-eftergivliga perikardiet begränsar den ventrikulära relaxationen och bestämmer det ventrikulära diastoliska trycket, vilket resulterar i förhöjda, utjämnade diastoliska tryck i alla kamrar. Kliniskt visar sig detta främst som högersidig kongestion (jugularvenös distension, ödem och ascites). Förhöjt tryck i det pulmonella kapillära kiltrycket och minskad hjärtminutvolym vid ansträngning (på grund av otillräcklig kammarfyllning) resulterar i dyspné och ansträngningsintolerans, även om ett öppet lungödem är mindre vanligt än typisk systolisk hjärtsvikt.
Det normala perikardiet reglerar kopplingen av vänster- och högersidiga slagvolymer under akuta förändringar i förbelastning, så att en plötslig ökning av högersidigt venöst återflöde (under inspiration) är förknippad med en vänstervridning av septum och en minskning av det transmurala fyllningstrycket i vänster ventrikel (LV) (LV diastoliskt tryck perikardietryck). Detta minskar i sin tur LV:s diastoliska slutvolym (LV-preload) och därmed den vänstersidiga slagvolymen.4 I det normala hjärtat är dessa förändringar i slagvolym vid andning minimala. Med en fast perikardiell volym i CP är den perikardiella kopplingen kraftigt överdriven, vilket leder till ett dramatiskt ventrikulärt ömsesidigt beroende. Onormal ventrikelseptalrörelse är ett resultat av förstärkta respirofasiska förändringar i vänster- och högersidig slagvolym.
I CP överförs den normala inspiratoriska minskningen av intrathorakaltrycket, på grund av att hjärtat är omslutet av ett icke-kompatibelt perikard, inte till intrakardialtrycket. Denna effekt förstärker inspiratoriska minskningar av det pulmonalvenösa trycket (eftersom lungvenerna i första hand är extraperikardiella), vilket översätts till en minskad vänstersidig inspiratorisk preload, vilket ytterligare minskar den vänstersidiga inspiratoriska slagvolymen. Multimodal diagnostisk utvärdering av CP lyfter fram dessa fynd och underlättar diagnosen.
Initialbedömning:
Den låga prevalensen av CP gör att identifiering av viktiga fysiska undersöknings- och historiska kännetecken är ett viktigt inledande steg i den diagnostiska processen. En historia av hjärtkirurgi, strålning eller tuberkulos bör öka den kliniska misstanken i närvaro av ödem, bukspridning och ansträngningsdyspné. Förhöjt jugular venous pressure (JVP) förekommer hos praktiskt taget alla patienter som inte är hypovolemiska. Perikardiell begränsning leder till att högerhjärtat inte kan tillgodose inspiratorisk bukvenös retur, vilket leder till en inspiratorisk ökning av JVP (Kussmauls tecken).5 De jugulära x- och y-avgångarna är framträdande vid CP, på grund av överdriven longitudinell ringrörelse respektive framträdande tidig ventrikelfyllning. I kontrast till detta uppvisar restriktiv kardiomyopati en avtrubbning av x-avsättningen på grund av försämrad förmaksrelaxation och förmaksmyopati. Vid auskultation kan man upptäcka en hög ton av perikardiell knackning längs den vänstra sternalgränsen. Ascites och betydande lägre ödem är vanliga och leder ofta till feldiagnos av leversjukdom om JVP-fynden inte känns igen.
Laboratoriska tester vid CP är ospecifika. Ett högt BNP kan antyda en större sannolikhet för restriktiv kardiomyopati, men studier har visat stor överlappning i diagnostiska värden i denna population vilket begränsar den kliniska användbarheten.6-9
Echokardiografi:
Som inledande diagnostiskt test kan ekokardiografi bekräfta diagnosen CP i de flesta fall om sannolikheten för pre-test är tillräckligt hög.10 Ekokardiografi visar drag av både överdrivet ventrikulärt interdependens och intrathorakal-intrakardiell dissociation. Det patognomoniska fyndet är respirofasisk septalförskjutning, som upptäcks med antingen M-mode eller 2D-bilddiagnostik.5 Förutom denna överdrivna respiratoriska septalrörelse finns det också en onormal septalrörelse från slag till slag, eller ”shudder”, på grund av differentiell snabb tidig diastolisk fyllning av höger och sedan vänster kammare.11 Den nedre vena cava är allmänt pletorisk i avsaknad av hypovolemi, vilket är ett känsligt men ospecifikt kännetecken för CP. Exspiratoriska leverveinomvändningar och minskat diastoliskt framåtflöde uppstår på grund av högerriktad ventrikelseptalrörelse till följd av en expiratorisk ökning av LV-preload, med en resulterande minskning av effektiv operativ högerkammarkomplexitet.
De överdrivna respiratoriska preloadförändringarna exemplifieras också av en inspiratorisk minskning av mitralisklaffens inflödesdoppler och en ökning av trikuspidalisklaffens inflödesdoppler. Dessa fynd är dock okänsliga. I närvaro av signifikant ökade kiltryck i vänster förmak och lungkapillärerna är minskningen av kiltryck-LV-gradienten vid inspiration otillräcklig för att förändra LV-preload tillräckligt mycket för att förändra mitrala inflödesdopplerstorleken12 . På grund av sidoväggsbindning är den laterala mitralringens tidiga diastoliska dopplerhastighet (e’) ofta minskad och onormalt lägre än den mediala e’-hastigheten (annulus reversus).13 Till skillnad från kardiomyopatiska orsaker till hjärtsvikt är den mediala e’-hastigheten relativt normal (eller till och med förhöjd, vilket kallas annulus paradoxus) med tanke på normal myokardisk relaxation och kompensatorisk longitudinell rörelse av den mediala mitralringen i samband med sidoväggsbindning.14,15
Hjärtröntgen:
I CP kan röntgenbilder av bröstkorgen påvisa perikardiell förkalkning, ett patognomoniskt fynd i närvaro av klinisk hjärtsvikt och förhöjt JVP. CT av bröstkorgen är känsligare för perikardiell förkalkning än röntgen av bröstkorgen.16 CT av bröstkorgen och MRT gör det möjligt att exakt mäta perikardtjockleken, och särskilt MRT visar utmärkt noggrannhet (93 %) när det gäller att upptäcka perikardtjocklek >4 mm.17 Det är dock viktigt att komma ihåg att upp till 18 % av fallen av kirurgiskt bekräftad CP kan ha normal perikardtjocklek trots patologisk avvikelse.18 Perikardiell tethering, som kan visualiseras via ekokardiografi, CT eller MRT kan också ge insikt om förekomsten av CP. MRT förmedlar information om aktiv perikardinflammation, vilket kan hjälpa till att vägleda terapeutiska beslut. Dessutom ger kardiell MRT en unik myokardiell bedömning, vilket kan identifiera kardiomyopatiska processer när diagnosen är osäker. Myokardiell fördröjd förstärkning saknas vanligtvis vid isolerad CP, men kan förekomma i nästan en tredjedel av fallen med restriktiv kardiomyopati.19
Till skillnad från ekokardiografi är hjärt-CT och MRT inte beroende av patientens habitus och kan ge bättre kardiell visualisering när ekkokardiografisk avbildning är suboptimal. Respirofasiska förskjutningar i septumrörelse påvisas väl på både CT och MRT. Dessutom kan CT och MRT ge information om alternativa orsaker till dyspné, t.ex. lungsjukdom eller diafragmatisk förlamning.
Diagnostik utöver kardiell avbildning:
Hjärtekateterisering förblir det diagnostiska testet som är guldstandard, om icke-invasiv testning inte är entydig, för att bedöma förekomst av förträngning och utvärdera hemodynamisk betydelse. Medan de flesta patienter med CP inte kräver hemodynamisk kateterisering för diagnos, är en undergrupp av särskilt intresse patienter med strålningshjärtsjukdom, hos vilka det ofta är svårt att identifiera graden av underliggande restriktiv kardiomyopati, även om konstriktiva drag är närvarande. Även med högkvalitativ ekokardiografi och hjärtröntgen kan dessa patienter kräva invasiv hemodynamisk kateterisering för att bedöma förhöjda fyllningstryck med diastolisk utjämning, ventrikulärt interdependens och intrathorakal-intrakardiell dissociation.2
Behandling:
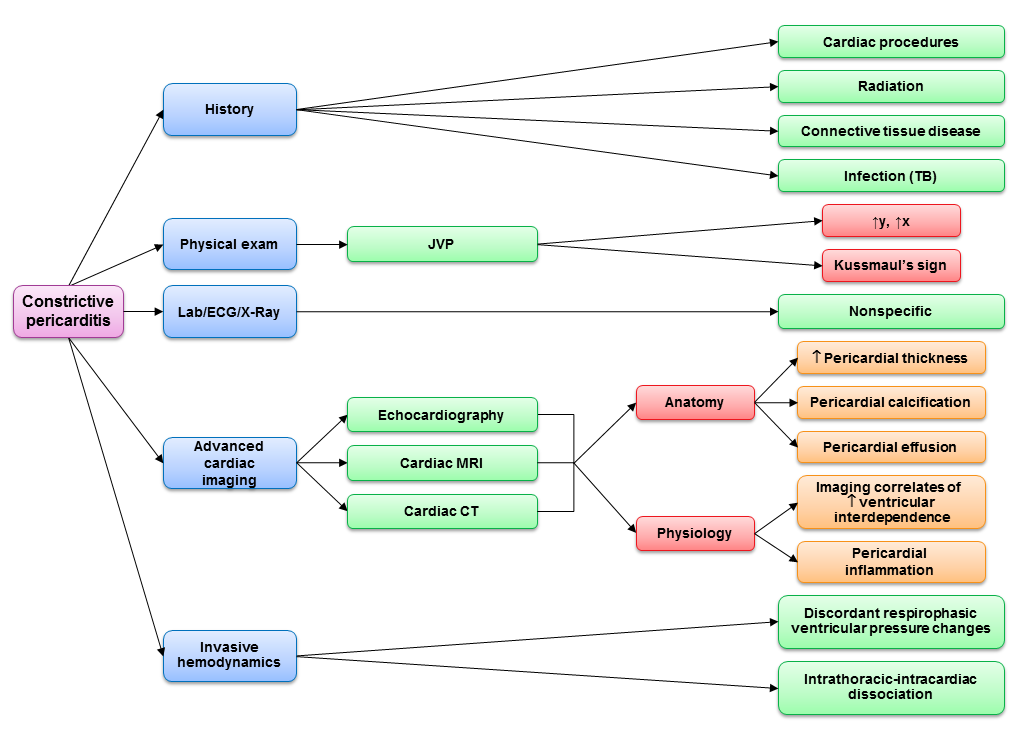
När CP väl har identifierats är medicinsk behandling med diures ofta bara delvis effektiv för att lindra symptomen. Om det finns omfattande perikardieinflammation är ett försök med antiinflammatorisk behandling motiverat för att bedöma om reversibilitet föreligger innan man går vidare med perikardiektomi. Vissa patienter kan få förbättrad följsamhet i perikardiet om de endast har en övergående förträngning på grund av inflammation.20 Kirurgisk fullständig perikardiektomi är indicerad för att lindra symtomen hos patienter med CP. Med hjälp av ett multimodalt diagnostiskt tillvägagångssätt (figur 1) är det numera ovanligt att patienterna går vidare till operationssalen för bekräftelse av CP. Med tanke på den ofta transformativa karaktären hos perikardiektomi för patienternas livskvalitet måste kliniker fortsätta att upprätthålla ett högt index av misstänksamhet för denna sällsynta men botbara form av hjärtsvikt.
Figur 1
- Imazio M, Brucato A, Maestroni S, et al. Risk för constrictive pericarditis efter akut perikardit. Circulation 2011;124:1270-5.
- Geske JB, Anavekar NS, Nishimura RA, Oh JK, Gersh BJ. Differentiering av konstriktion och restriktion: komplex kardiovaskulär hemodynamik. J Am Coll Cardiol 2016;68:2329-47.
- Ling LH, Oh JK, Schaff HV, et al. Constrictive pericarditis in the modern era: evolving clinical spectrum and impact on outcome after pericardiectomy. Circulation 1999;100:1380-6.
- Kroeker CA, Shrive NG, Belenkie I, Tyberg JV. Perikardiet modulerar vänster och höger ventrikulära slagvolymer för att kompensera för plötsliga förändringar i förmaksvolymen. Am J Physiol Heart Circ Physiol 2003;284:H2247-54.
- Talreja DR, Nishimura RA, Oh JK, Holmes DR. Constrictive pericarditis in the modern era: nya kriterier för diagnos i hjärtkateteriseringslaboratoriet. J Am Coll Cardiol 2008;51:315-9.
- Sengupta PP, Krishnamoorthy VK, Abhayaratna WP, et al. Comparison of usefulness of tissue doppler imaging versus brain natriuretic peptide for differentiation of constrictive pericardial disease from restrictive cardiomyopathy. Am J Cardiol 2008;102:357-62.
- Leya FS, Arab D, Joyal D, et al. The efficacy of brain natriuretic peptide levels in differentiating constrictive pericarditis from restrictive cardiomyopathy. J Am Coll Cardiol 2005;45:1900-2.
- Babuin L, Alegria JR, Oh JK, Nishimura RA, Jaffe AS. Nivåer av natriuretisk peptid i hjärnan vid konstriktiv perikardit och restriktiv kardiomyopati. J Am Coll Cardiol 2006;47:1489-91.
- Reddy PR, Dieter RS, Das P, Steen LH, Lewis BE, Leya FS. Nyttan av BNP för att skilja konstriktiv perikardit från restriktiv kardiomyopati hos patienter med njurinsufficiens. J Card Fail 2007;13:668-71.
- Welch TD, Ling LH, Espinosa RE, et al. Echocardiographic diagnosis of constrictive pericarditis: Mayo Clinic-kriterier. Circ Cardiovasc Imaging 2014;7:526-34.
- Coylewright M, Welch TD, Nishimura RA. Mekanism för septalbounce vid constrictive pericarditis: en samtidig studie med hjärtkateterisering och ekokardiografi. Heart 2013;99:1376.
- Oh JK, Tajik AJ, Appleton CP, Hatle LK, Nishimura RA, Seward JB. Reduktion av förbelastningen för att avmaska de karakteristiska doppleregenskaperna vid constrictiv perikardit: en ny observation. Circulation 1997;95:796-9.
- Reuss CS, Wilansky SM, Lester SJ, et al. Användning av mitral ”annulus reversus” för att diagnostisera constrictive perikardit. Eur J Echocardiogr 2009;10:372-5.
- Ha JW, Oh JK, Ling LH, Nishimura RA, Seward JB, Tajik AJ. Annulus paradoxus: förhållandet mellan transmittral flödeshastighet och mitralringens hastighet är omvänt proportionellt mot det pulmonella kapillära kiltrycket hos patienter med konstriktiv perikardit. Circulation 2001;104:976-8.
- Ha JW, Ommen SR, Tajik AJ, et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue doppler echocardiography. Am J Cardiol 2004;94:316-9.
- Ling LH, Oh JK, Breen JF, et al. Calcific constrictive pericarditis: is it still with us? Ann Intern Med 2000;132:444-50.
- Masui T, Finck S, Higgins CB. Konstriktiv perikardit och restriktiv kardiomyopati: utvärdering med MR-avbildning. Radiology 1992;182:369-73.
- Talreja DR, Edwards WD, Danielson GK, et al. Constrictive pericarditis in 26 patients with histologically normal pericardial thickness. Circulation 2003;108:1852-7.
- Muehlberg F, Toepper A, Fritschi S, Prothmann M, Schulz-Menger J. Magnetic resonance imaging applications on infiltrative cardiomyopathies. J Thorac Imaging 2016;31:336-47.
- Haley JH, Tajik AJ, Danielson GK, Schaff HV, Mulvagh SL, Oh JK. Transient constrictive pericarditis: orsaker och naturlig historia. J Am Coll Cardiol 2004;43:271-5.
Kliniska ämnen: Hjärtkirurgi, Hjärtsvikt och kardiomyopatier, Invasiv kardiovaskulär angiografi och intervention, Icke-invasiv avbildning, Perikardsjukdom, Hjärtkirurgi och hjärtsvikt, Akut hjärtsvikt, Kronisk hjärtsvikt, Interventioner och avbildning, Datortomografi, Ekokardiografi/Ultraljud, Nukleär avbildning
Nyckelord: Blodtryck, hjärtkateterisering, kardiomyopati, restriktiv, diagnostiska fel, diagnostiska tester, rutin, diures, dyspné, ekokardiografi, ödem, hjärtsvikt, systolisk, hjärtkamrar, hepatiska vener, hypovolemi, mitralisklaffen, perikardiektomi, Perikardit, konstriktiv, Perikard, Lungödem, Lungavener, Pulmonary Wedge Pressure, Trikuspidalventilen, Tomografi, röntgenkomputerad, Vena Cava, Inferior, Venous Pressure, Ventricular Pressure, X-Rays
< Tillbaka till listorna