La pericardite costrittiva (CP) è una forma relativamente poco comune di insufficienza cardiaca clinica. La vera prevalenza nella popolazione è sconosciuta, ma tra coloro che hanno una pericardite virale è stato stimato che si verifica in meno dello 0,5% dei casi.1 Tuttavia, poiché è potenzialmente reversibile, la diagnosi non deve essere mancata. La pericardectomia chirurgica ha la capacità di “curare” la CP, con notevoli miglioramenti dei sintomi e della qualità della vita.2,3 Anche se l’eziologia della CP può essere varia (idiopatica, post virale, tubercolosa, post chirurgica, indotta da radiazioni, ecc.), la via comune finale è lo sviluppo di ispessimento fibroso o calcificazione del pericardio con conseguente non conformità pericardica.
Fisiologia e fisiopatologia pericardica nella costrizione:
Il pericardio normale ostacola minimamente la distensibilità ventricolare a volumi operativi cardiaci normali. Nella CP, la non conformità pericardica crea un’unità ventricolare-pericardica rigida, portando ad un aumento delle pressioni diastoliche e ad un aumento più rapido delle pressioni ventricolari per un dato ritorno venoso. Il pericardio non conforme limita il rilassamento ventricolare e determina la pressione diastolica ventricolare, determinando pressioni diastoliche elevate ed eguagliate in tutte le camere. Clinicamente, questo si presenta prevalentemente come congestione del lato destro (distensione venosa giugulare, edema e ascite). L’elevazione della pressione di cuneo capillare polmonare e una diminuzione della risposta della gittata cardiaca all’esercizio (dato il riempimento ventricolare inadeguato) si traduce in dispnea e intolleranza allo sforzo, anche se l’edema polmonare franco è meno comune della tipica insufficienza cardiaca sistolica.
Il pericardio normale regola l’accoppiamento dei volumi di ictus lato sinistro e destro durante i cambiamenti acuti nel precarico, in modo tale che un improvviso aumento del ritorno venoso lato destro (durante l’ispirazione) è associato con arco settale verso sinistra e una diminuzione del ventricolo sinistro (LV) pressione di riempimento transmurale (pressione diastolica LV pressione pericardica). Questo a sua volta diminuisce il volume diastolico finale del LV (precarico LV) e quindi il volume di ictus del lato sinistro.4 Nel cuore normale, questi cambiamenti nel volume di ictus con la respirazione sono minimi. Dato un volume pericardico fisso in CP, l’accoppiamento pericardico è notevolmente esagerato, portando a una drammatica interdipendenza ventricolare. Il movimento anormale del setto ventricolare risulta da alterazioni respirofasiche potenziate nel volume dell’ictus dei lati destro e sinistro.
In CP, a causa del cuore racchiuso da un pericardio non flessibile, la normale diminuzione inspiratoria della pressione intratoracica non viene trasmessa alle pressioni intracardiache. Questo effetto amplifica le diminuzioni inspiratorie nella pressione venosa polmonare (dal momento che le vene polmonari sono principalmente extrapericardico), traducendo in un precarico inspiratorio ridotto lato sinistro, riducendo ulteriormente il volume inspiratorio lato sinistro colpo. La valutazione diagnostica multimodale di CP evidenzia questi risultati, facilitando la diagnosi.
Valutazione iniziale:
La bassa prevalenza di CP rende l’identificazione dell’esame fisico chiave e le caratteristiche storiche un importante passo iniziale nel processo diagnostico. Una storia di chirurgia cardiaca, radiazioni o tubercolosi dovrebbe aumentare il sospetto clinico in presenza di edema, distensione addominale e dispnea da sforzo. La pressione venosa giugulare elevata (JVP) è presente praticamente in tutti i pazienti che non sono ipovolemici. La costrizione pericardica si traduce nell’incapacità del cuore destro di accogliere il ritorno venoso addominale inspiratorio, traducendosi in un aumento inspiratorio della JVP (segno di Kussmaul).5 Le discese giugulari x e y sono prominenti nella CP, a causa di un esagerato movimento anulare longitudinale e di un prominente riempimento ventricolare iniziale, rispettivamente. Al contrario, la cardiomiopatia restrittiva dimostra l’attenuazione della discesa x, a causa della compromissione del rilassamento atriale e della miopatia atriale. L’auscultazione può rivelare un colpo pericardico acuto lungo il bordo sternale sinistro. L’ascite e il significativo edema inferiore sono comuni e spesso portano alla diagnosi errata di malattia epatica se i risultati JVP non sono riconosciuti.
I test di laboratorio in CP non sono specifici. Un BNP elevato può suggerire una maggiore probabilità di cardiomiopatia restrittiva, ma gli studi hanno mostrato grande sovrapposizione nei valori diagnostici in questa popolazione limitando l’utilità clinica.6-9
Ecocardiografia:
Come un test diagnostico iniziale, ecocardiografia può confermare la diagnosi di CP nella maggior parte dei casi se la probabilità pre-test è sufficientemente alta.10 Ecocardiografia dimostra caratteristiche di entrambi esagerata interdipendenza ventricolare e dissociazione intratoracica-intracardiaca. Il reperto patognomonico è lo spostamento respirofasico del setto, rilevato sia dalla modalità M che dall’imaging 2D.5 Oltre a questo esagerato movimento respiratorio del setto, c’è anche un movimento anomalo del setto da battito a battito, o “shudder”, dovuto al rapido riempimento diastolico differenziale iniziale del ventricolo destro e poi di quello sinistro.11 La vena cava inferiore è universalmente pletorica in assenza di ipovolemia; una caratteristica sensibile ma aspecifica della CP. Le inversioni della vena epatica espiratoria e la diminuzione del flusso diastolico in avanti si verificano a causa del movimento del setto ventricolare verso destra da un aumento espiratorio nel precarico LV, con una conseguente diminuzione della compliance effettiva operativo ventricolare destro.
I cambiamenti esagerati precarico respiratorio sono anche esemplificati da una diminuzione inspiratoria in afflusso valvola mitrale Doppler e un aumento della valvola tricuspide afflusso Doppler. Tuttavia, questi risultati sono insensibili. In presenza di atriale sinistro significativamente aumentato e pressioni capillari polmonari cuneo, la diminuzione della pressione cuneo-LV gradiente con ispirazione è insufficiente per cambiare precarico LV abbastanza per alterare la grandezza Doppler afflusso mitrale.12 A causa di tethering parete laterale, l’anulus mitrale laterale velocità diastolica precoce tessuto Doppler (e ‘) è spesso diminuita e anormalmente inferiore alla velocità mediale e ‘ (annulus reversus).13 In contrasto con le cause cardiomiopatiche di insufficienza cardiaca, la velocità mediale e ‘è relativamente normale (o addirittura aumentato, chiamato paradosso annulus) dato normale rilassamento miocardico e compensativo movimento longitudinale anulare mediale in impostazione di tethering parete laterale.14,15
Radiologia cardiaca:
Nella CP, i raggi x del torace possono dimostrare la calcificazione pericardica, un reperto patognomonico in presenza di insufficienza cardiaca clinica e JVP elevata. La TC del torace è più sensibile alla calcificazione pericardica rispetto alla radiografia del torace.16 La TC del torace e la RM permettono una misurazione precisa dello spessore pericardico, con la RM in particolare che dimostra un’eccellente accuratezza (93%) nel rilevamento dell’ispessimento pericardico >4 mm.17 Tuttavia, è importante ricordare che fino al 18% dei casi di CP confermata chirurgicamente può avere uno spessore pericardico normale nonostante la non conformità patologica.18 Anche il tethering pericardico, che può essere visualizzato tramite ecocardiografia, TC o RM può fornire informazioni sulla presenza di CP. La risonanza magnetica fornisce informazioni sull’infiammazione pericardica attiva, che può aiutare a guidare le decisioni terapeutiche. Inoltre, la risonanza magnetica cardiaca fornisce una valutazione miocardica unica, che può identificare i processi cardiomiopatici quando la diagnosi è incerta. L’incremento miocardico ritardato è tipicamente assente nella CP isolata, ma può verificarsi in quasi un terzo dei casi con cardiomiopatia restrittiva.19
A differenza dell’ecocardiografia, la TC e la RM cardiaca non dipendono dall’abitudine del paziente e possono fornire una migliore visualizzazione cardiaca quando l’imaging ecocardiografico non è ottimale. Gli spostamenti respirofasici nel movimento del setto sono ben dimostrati sia sulla CT che sulla MRI. Inoltre, CT e MRI può fornire informazioni su cause alternative di dispnea come la malattia polmonare o paralisi diaframmatica.
Diagnosi oltre imaging cardiaco:
Cateterismo cardiaco rimane il test diagnostico gold standard, se test non invasivo è inconcludente, per valutare la presenza di costrizione e valutare il significato emodinamico. Mentre la maggior parte dei pazienti con CP non richiedono cateterismo emodinamico per la diagnosi, un sottogruppo di particolare preoccupazione è pazienti con malattia cardiaca di radiazione, in cui è spesso difficile identificare il grado di sottostante cardiomiopatia restrittiva, anche se sono presenti caratteristiche costrittive. Anche con ecocardiografia e radiologia cardiaca di alta qualità, questi pazienti possono richiedere un cateterismo emodinamico invasivo per valutare l’elevazione delle pressioni di riempimento con equalizzazione diastolica, interdipendenza ventricolare e dissociazione intratoracica-intracardiaca.2
Trattamento:
Una volta identificata la CP, il trattamento medico con diuresi è spesso solo parzialmente efficace nel palliare i sintomi. Se c’è un’estesa infiammazione pericardica, una prova di terapia antinfiammatoria è giustificata per valutare la reversibilità prima di procedere con la pericardiectomia. Alcuni pazienti possono avere un miglioramento della compliance pericardica se hanno solo una costrizione transitoria dovuta all’infiammazione.20 La pericardiectomia chirurgica completa è indicata per alleviare i sintomi nei pazienti con CP. Utilizzando un approccio diagnostico multimodale (Figura 1), è ormai raro che i pazienti debbano procedere in sala operatoria per la conferma della CP. Data la natura spesso trasformativa della pericardiectomia per la qualità della vita dei pazienti, i medici devono continuare a mantenere un alto indice di sospetto per questa rara ma curabile forma di insufficienza cardiaca.
Figura 1
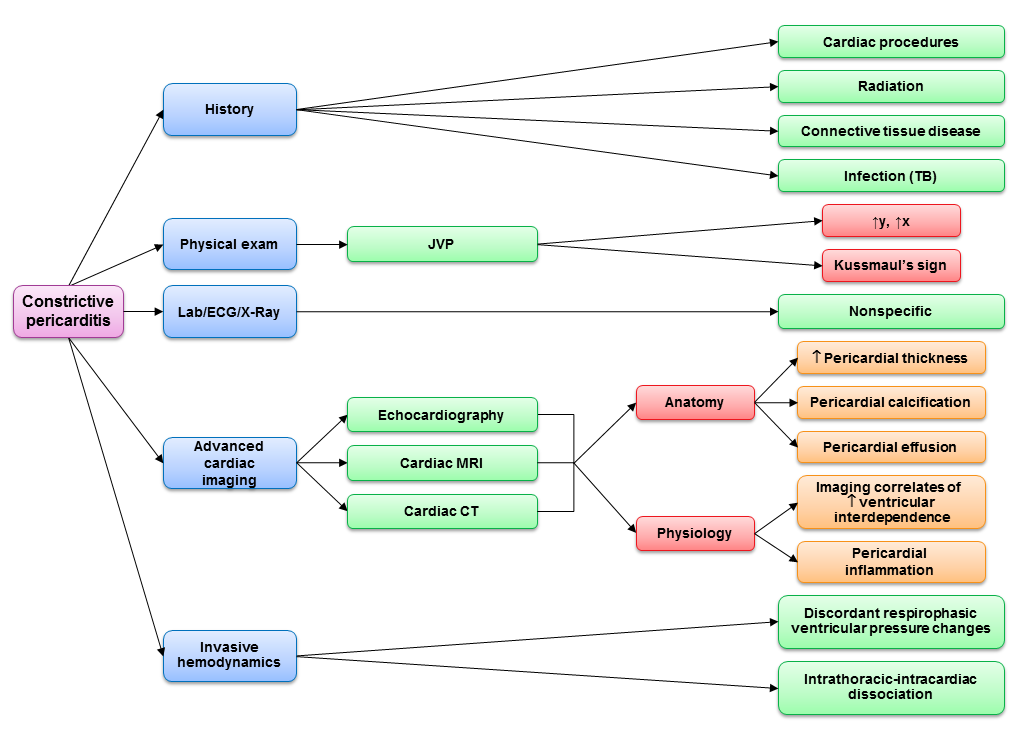
- Imazio M, Brucato A, Maestroni S, et al. Rischio di pericardite costrittiva dopo pericardite acuta. Circulation 2011;124:1270-5.
- Geske JB, Anavekar NS, Nishimura RA, Oh JK, Gersh BJ. Differenziazione di costrizione e restrizione: emodinamica cardiovascolare complessa. J Am Coll Cardiol 2016;68:2329-47.
- Ling LH, Oh JK, Schaff HV, et al. Pericardite costrittiva nell’era moderna: spettro clinico in evoluzione e impatto sul risultato dopo pericardiectomia. Circulation 1999;100:1380-6.
- Kroeker CA, Shrive NG, Belenkie I, Tyberg JV. Pericardio modula i volumi di corsa ventricolare sinistra e destra per compensare i cambiamenti improvvisi nel volume atriale. Am J Physiol Heart Circ Physiol 2003;284:H2247-54.
- Talreja DR, Nishimura RA, Oh JK, Holmes DR. Pericardite costrittiva nell’era moderna: nuovi criteri per la diagnosi nel laboratorio di cateterizzazione cardiaca. J Am Coll Cardiol 2008;51:315-9.
- Sengupta PP, Krishnamoorthy VK, Abhayaratna WP, et al. Confronto dell’utilità dell’imaging Doppler del tessuto rispetto al peptide natriuretico del cervello per la differenziazione della malattia pericardica costrittiva dalla cardiomiopatia restrittiva. Am J Cardiol 2008;102:357-62.
- Leya FS, Arab D, Joyal D, et al. L’efficacia dei livelli di peptide natriuretico del cervello nel differenziare la pericardite costrittiva dalla cardiomiopatia restrittiva. J Am Coll Cardiol 2005;45:1900-2.
- Babuin L, Alegria JR, Oh JK, Nishimura RA, Jaffe AS. Livelli di peptide natriuretico cerebrale in pericardite costrittiva e cardiomiopatia restrittiva. J Am Coll Cardiol 2006;47:1489-91.
- Reddy PR, Dieter RS, Das P, Steen LH, Lewis BE, Leya FS. Utilità del BNP nel differenziare la pericardite costrittiva dalla cardiomiopatia restrittiva nei pazienti con insufficienza renale. J Card Fail 2007;13:668-71.
- Welch TD, Ling LH, Espinosa RE, et al. Diagnosi ecocardiografica di pericardite costrittiva: Criteri della Mayo Clinic. Circ Cardiovasc Imaging 2014;7:526-34.
- Coylewright M, Welch TD, Nishimura RA. Meccanismo di rimbalzo settale in pericardite costrittiva: uno studio simultaneo di cateterismo cardiaco ed ecocardiografico. Cuore 2013;99:1376.
- Oh JK, Tajik AJ, Appleton CP, Hatle LK, Nishimura RA, Seward JB. Riduzione del precarico per smascherare le caratteristiche Doppler della pericardite costrittiva: una nuova osservazione. Circulation 1997;95:796-9.
- Reuss CS, Wilansky SM, Lester SJ, et al. Utilizzando mitrale ‘annulus reversus’ per diagnosticare pericardite costrittiva. Eur J Echocardiogr 2009;10:372-5.
- Ha JW, Oh JK, Ling LH, Nishimura RA, Seward JB, Tajik AJ. Annulus paradoxus: il rapporto tra la velocità del flusso transmitrale e la velocità anulare mitrale è inversamente proporzionale alla pressione di cuneo capillare polmonare in pazienti con pericardite costrittiva. Circulation 2001;104:976-8.
- Ha JW, Ommen SR, Tajik AJ, et al. Differenziazione di pericardite costrittiva da cardiomiopatia restrittiva utilizzando la velocità anulare mitrale da ecocardiografia Doppler del tessuto. Am J Cardiol 2004;94:316-9.
- Ling LH, Oh JK, Breen JF, et al. Pericardite costrittiva calcifica: è ancora con noi? Ann Intern Med 2000;132:444-50.
- Masui T, Finck S, Higgins CB. Pericardite costrittiva e cardiomiopatia restrittiva: valutazione con imaging MR. Radiologia 1992;182:369-73.
- Talreja DR, Edwards WD, Danielson GK, et al. pericardite costrittiva in 26 pazienti con spessore pericardico istologicamente normale. Circulation 2003;108:1852-7.
- Muehlberg F, Toepper A, Fritschi S, Prothmann M, Schulz-Menger J. Applicazioni di risonanza magnetica su cardiomiopatie infiltrative. J Thorac Imaging 2016;31:336-47.
- Haley JH, Tajik AJ, Danielson GK, Schaff HV, Mulvagh SL, Oh JK. Pericardite costrittiva transitoria: cause e storia naturale. J Am Coll Cardiol 2004;43:271-5.
Temi clinici: Chirurgia cardiaca, Insufficienza cardiaca e cardiomiopatie, Angiografia e intervento cardiovascolare invasivo, Imaging non invasivo, Malattia pericardica, Chirurgia cardiaca e insufficienza cardiaca, Insufficienza cardiaca acuta, Insufficienza cardiaca cronica, Interventi e Imaging, Tomografia computerizzata, Ecocardiografia/Ultrasuoni, Imaging nucleare
Keywords: Pressione sanguigna, Cateterismo cardiaco, Cardiomiopatia, Restrittiva, Errori diagnostici, Test diagnostici, Routine, Diuresi, Dispnea, Ecocardiografia, Edema, Insufficienza cardiaca, Sistolico, Ventricoli cardiaci, Vene epatiche, Ipovolemia, Valvola mitrale, Pericardiectomia, Pericardite costrittiva, Pericardio, Edema polmonare, Vene polmonari, Pressione di incuneamento polmonare, Valvola tricuspide, Tomografia computerizzata a raggi X, Vena cava inferiore, Pressione venosa, Pressione ventricolare, Raggi X
< Torna alle inserzioni