- Schwefeltrioxid Chemische Eigenschaften, Verwendung, Herstellung
- Chemische Eigenschaften
- Physikalische Eigenschaften
- Verwendungen
- Herstellungsmethoden
- Allgemeine Beschreibung
- Luft &Wasserreaktionen
- Reaktivitätsprofil
- Gefahr
- Gesundheitsgefährdung
- Brandgefahr
- Sicherheitsprofil
- Potenzielle Exposition
- Lagerung
- Versand
- Unverträglichkeiten
- Abfallentsorgung
Schwefeltrioxid Chemische Eigenschaften, Verwendung, Herstellung
Chemische Eigenschaften
Schwefeltrioxid, S03, auch bekannt als Schwefelsäureanhydrid, Nadeln oder Polymer, existiert in einer Reihe von Modifikationen, die sich in Molekülart und kristalliner Form unterscheiden. Es gibt eine weiße, eisähnliche Modifikation, die bei 16 °C schmilzt, und zwei weitere, bestienähnliche Formen, die bei höheren Temperaturen von 33 und 62 °C schmelzen. Die farblose flüssige oder gasförmige Form hat reizende, giftige Dämpfe und siedet bei 45 °C.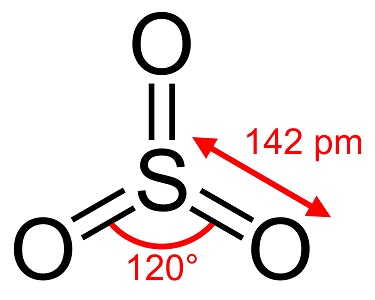
Schwefeltrioxid ist ein hochreaktiver Stoff, ein starkes Oxidationsmittel und eine Brandgefahr. Es reagiert mit Metalloxiden unter Bildung von Sulfaten und mit Wasser unter Bildung von Schwefelsäure. Schwefeltrioxid wird zur Sulfonierung verwendet.
Physikalische Eigenschaften
Farblose Flüssigkeit bei Umgebungstemperatur und Atmosphärendruck; Dämpfe an der Luft.
Schwefeltrioxid neigt zur Polymerisation, insbesondere in Gegenwart von Spuren von Wasser oder Schwefelsäure. Die Polymerisationsgeschwindigkeit nimmt jedoch bei Annäherung an den Gefrierpunkt stark ab. Festes (polymeres) Schwefeltrioxid liegt in drei polymorphen Phasen vor: Alpha-, Beta- und Gamma-Modifikationen.
Die Alpha-Phase besteht aus eisähnlichen Nadeln mit polymerer Vernetzungsstruktur. Sie schmilzt bei 62,3°C und hat einen Dampfdruck von 73 Torr bei 25°C.
Die Beta-Phase ist ein metastabiles Allotrop mit weißen, asbestartigen, glänzenden Nadeln, die aus Polymermolekülen bestehen, bei 32,5°C schmelzen und einen Dampfdruck von 344 Torr bei 25°C haben.
Die Gamma-Modifikation kann bei normalen Temperaturen in fester oder flüssiger Form vorliegen. In fester Form ist sie eine kolloidale eisähnliche Masse, die bei 16,8°C schmilzt. In flüssiger Form hat sie eine Dichte von 1,9224 g/ml und siedet bei 44,8°C. Es hat einen Dampfdruck von 433 Torr bei 25°C. Die Gamma-Phase besteht sowohl aus zyklischen Trimeren als auch aus Monomermolekülen. Wenn festes Schwefeltrioxid schmilzt, wandelt es sich in seine Gamma-Phase um, die bei der Verfestigung in die Alpha-Modifikation übergeht.
Die kritische Temperatur von SO3 beträgt 217,8°C; der kritische Druck 80,97 atm; die kritische Dichte 0,63 g/cm3; die Dielektrizitätskonstante von flüssigem SO3 bei 18°C beträgt 3,11.
Schwefeltrioxid löst sich in Wasser unter Bildung von Schwefelsäure und großer Wärmeentwicklung.
Verwendungen
Schwefeltrioxid wird als Zwischenprodukt bei der Herstellung von Schwefelsäure und Oleum für die Sulfonierung, insbesondere von Farbstoffen und Färbemitteln, sowie für die Herstellung von wasserfreier Salpetersäure und Sprengstoffen verwendet. Festes Schwefeltrioxid wird unter Bezeichnungen wie Sulphan und Triosul vermarktet und hauptsächlich zur Sulfonierung organischer Säuren verwendet. Schwefeltetrafluorid ist ein Fluorierungsmittel. Schwefelhexafluorid dient als gasförmiger Isolator in elektrischen Hochspannungsanlagen. Sulphyrylfluorid wird als Insektizid und Begasungsmittel verwendet.
Sulfonierung organischer Verbindungen, insbesondere nichtionische Detergenzien, Sonnenenergiekollektoren. Es wird in der Regel in dem Betrieb erzeugt, in dem es verwendet werden soll.
Herstellungsmethoden
Schwefeltrioxid wird als Zwischenprodukt bei der Herstellung von Schwefelsäure nach dem Kontaktverfahren hergestellt (siehe Schwefelsäure). Das Verfahren beinhaltet die katalytische Oxidation von Schwefeldioxid zu Trioxid.
Schwefeltrioxid wird im Labor durch Erhitzen rauchender Schwefelsäure, Kondensation der Dämpfe und Auffangen in einem kühlen Behälter hergestellt. Wenn die Dämpfe in Gegenwart von Spuren von Feuchtigkeit unter 27 °C kondensiert werden, entstehen alle drei polymorphen Phasen von SO3. Sie können durch fraktionierte Destillation getrennt werden. Bei der Kondensation der Dämpfe über 27 °C entsteht die flüssige Variante des Gamma-Schwefeltrioxids.
Allgemeine Beschreibung
Schwefeltrioxid ist ein farbloser bis weißer kristalliner Feststoff, der an der Luft dampft. Es wird oft mit einem Inhibitor geliefert, um die Polymerisation zu verhindern. Schwefeltrioxid reagiert heftig mit Wasser und bildet unter Wärmeentwicklung Schwefelsäure. Schwefeltrioxid ist ätzend für Metalle und Gewebe. Schwefeltrioxid verursacht Augen- und Hautverätzungen. Verschlucken führt zu schweren Verätzungen der Speiseröhre und des Magens. Die Dämpfe sind beim Einatmen sehr giftig. Schwefeltrioxid stellt eine Brandgefahr dar, wenn es mit organischen Materialien wie Holz, Baumwolle, Faserplatten usw. in Berührung kommt.
Luft &Wasserreaktionen
Verbindet sich mit Wasser mit explosiver Kraft und bildet aufgrund seiner Säure Schwefelsäure Schwefeltrioxid verkohlt die meisten organischen Stoffe. An der Luft absorbiert Schwefeltrioxid schnell Feuchtigkeit und gibt dichte weiße Dämpfe ab.
Reaktivitätsprofil
Die Reaktion von Schwefeltrioxid und Sauerstoffdifluorid ist sehr heftig und es kommt zu Explosionen, wenn die Reaktion ohne Lösungsmittel durchgeführt wird. Die Reaktion von Schwefeltrioxid im Überschuss mit Tetrafluorethylen führt zu einer explosiven Zersetzung zu Carbonylfluorid und Schwefeldioxid. Die Reaktion von wasserfreier Perchlorsäure mit Schwefeltrioxid ist heftig und geht mit einer erheblichen Wärmeentwicklung einher (Pascal 16:300 1931-34). Flüssiges Schwefeltrioxid reagiert auch bei 75 °C heftig mit Nitrylchlorid. Die Reaktion von Schwefeltrioxid mit Bleioxid führt zu weißer Lumineszenz. Die Kombination von Jod, Pyridin, Schwefeltrioxid und Formamid entwickelte nach einigen Monaten einen Gasüberdruck. Dies ist auf die langsame Bildung von Schwefelsäure, von äußerem Wasser oder die Dehydratisierung des Formamids zu Blausäure zurückzuführen.
Gefahr
Oxidationsmittel, Brandgefahr bei Kontakt mit anorganischen Materialien, beim Schmelzen der α-Form kommt es zu einem explosionsartigen Anstieg des Dampfdrucks. Das Anhydrid verbindet sich mit Wasser unter Bildung von Schwefelsäure und Wärmeentwicklung. Sehr giftig, stark reizend für das Gewebe.
Gesundheitsgefährdung
Schwefeltrioxid ist hochgiftig. Es ist reizend und ätzend für die Schleimhäute. Giftig beim Einatmen oder Verschlucken. Kontakt verursacht schwere Verätzungen an Haut und Augen.
Brandgefahr
Brandgefahr bei Kontakt mit organischen Materialien. Beim Schmelzen der Alpha-Form kommt es zu einem explosionsartigen Anstieg des Dampfdrucks. Verbindet sich mit Wasser mit explosiver Gewalt und bildet Schwefelsäure. Kann andere brennbare Materialien (Holz, Papier, Öl usw.) entzünden. Entflammbare giftige Gase können sich in Tanks und Trichterwagen ansammeln. Abfluss in die Kanalisation kann zu Brand- oder Explosionsgefahr führen. Bildet bei Kontakt mit Wasser Schwefelsäure. Wasser und organische Materialien meiden. Bei Kontakt mit der Luft absorbiert Schwefeltrioxid Feuchtigkeit und gibt dichte weiße Dämpfe ab.
Sicherheitsprofil
Giftig beim Einatmen. Systemische Wirkungen beim Menschen durch Einatmen: Husten und andere pulmonale und olfaktorische Veränderungen. Ätzende Reizung von Haut, Augen und Schleimhäuten. Heftige Reaktion mit O2F2, PbO, NClO2, HClO4, P, Tetrafluorethylen, Acetonitril, Schwefelsäure, Dimethylsulfoxid, Dioxan, Wasser, Diphenylquecksilber, Formamid, Jod, Pyridin, Metalloxiden. Reagiert mit Wasserdampf und bildet ätzende, giftige Schwefelsäuredämpfe. Beim Erhitzen bis zur Zersetzung werden giftige SO, -Rauchgase freigesetzt. Siehe auch SULFURIC ACID.
Potenzielle Exposition
Schwefeltrioxid wird als Sulfatierungs- und Sulfonierungsmittel für Reinigungsmittel, Schmieröladditive und andere organische Verbindungen sowie in Sonnenenergiekollektoren verwendet. Es wird auch als Zwischenprodukt bei der Herstellung von Schwefelsäure und bei der Herstellung von Sprengstoffen verwendet.
Lagerung
Der Dampfdruck von Schwefeltrioxid steigt mit zunehmender Temperatur rasch an, und wenn die α-Form schmilzt, ist der Druckanstieg explosiv; daher müssen Transport- und Lagerbehälter einem Druck von 10 bis 15 atm standhalten. Schwefeltrioxid reagiert heftig und stark exotherm mit Wasser unter Bildung von Schwefelwasserstoffsäure. An feuchter Luft raucht es und bildet einen Schwefelsäurenebel, der schließlich den gesamten verfügbaren Raum ausfüllt; außerdem korrodiert es Metalle. Sie ist ein starkes Oxidationsmittel und verkohlt in der flüssigen Phase organische Materialien.
Versand
UN1829 Schwefeltrioxid, stabilisiert, Gefahrenklasse: 8; Kennzeichnungen: 8-Ätzendes Material, 6.1-Giftige Gefahr beim Einatmen, Gefahrenzone B.
Unverträglichkeiten
Brennbar und ätzend. Ein starkes Oxidationsmittel. Reagiert heftig mit Wasser, Dampf oder Feuchtigkeit und setzt dabei ätzende Schwefelwasserstoffsäure frei. Heftige Reaktionen treten auf bei Kontakt mit starken Basen, starken Säuren, chemisch aktiven Metallen, Reduktionsmitteln, fein verteilten Metallen, Cyaniden, Nitraten, Pikraten, Fulminaten, Chloraten, Sulfiden, Carbiden, Phosphor, Dioxygendifluorid, Bariumoxid, Bleioxid, Diphenylquecksilber, Alkoholen, Nitrylchlorid, Acetonitril, Dioxan, Tetrafluorethylen.
Abfallentsorgung
Wiederbefüllbare Druckgasflaschen an den Lieferanten zurückgeben. Nicht nachfüllbare Gasflaschen sind gemäß den örtlichen, staatlichen und bundesstaatlichen Vorschriften zu entsorgen. Das verbleibende Gas in einem nicht abgeschlossenen Bereich oder einer Abzugshaube langsam in die Atmosphäre entweichen lassen. Wiederbefüllbare Druckgasflaschen sollten an den ursprünglichen Lieferanten zurückgegeben werden, wobei alle Ventilkappen und Auslassstopfen gesichert und die Ventilschutzkappen angebracht sein sollten.