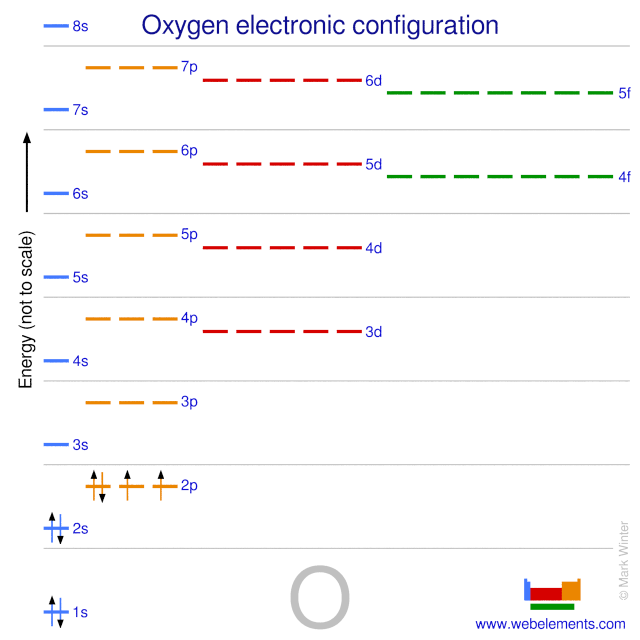
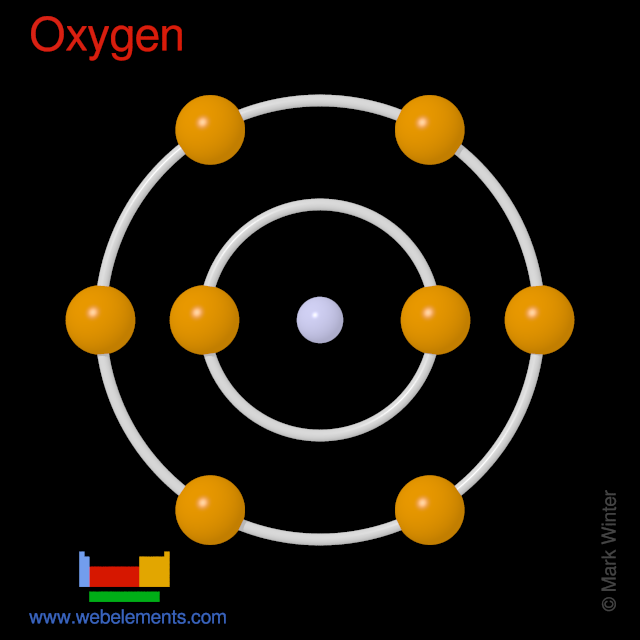
Sauerstoffatome haben 8 Elektronen und die Schalenstruktur ist 2.6.
Die Grundzustandselektronenkonfiguration von gasförmigem, neutralem Sauerstoff ist .2s2.2p4 und das Termsymbol ist 3P2.
Atomspektrum
Eine Darstellung des Atomspektrums von Sauerstoff.
Ionisierungsenergien und Elektronenaffinität
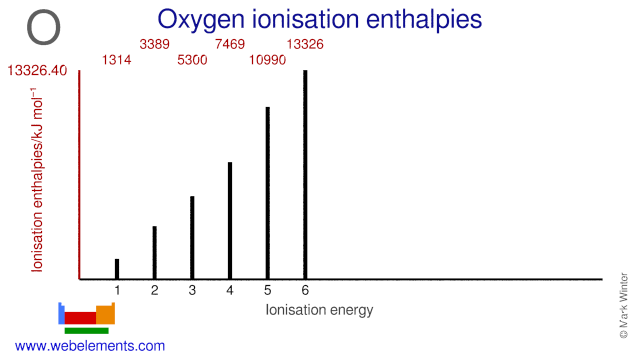
Die Elektronenaffinität von Sauerstoff beträgt 141 kJ mol-1. Die Ionisierungsenergien von Sauerstoff sind unten angegeben.
| Ionisierungsenergienummer | Enthalpie / kJ mol-1 |
|---|---|
| 1st | 1313.94 |
| 2. | 3388.67 |
| 3. | 5300.47 |
| 4. | 7469.27 |
| 5te | 10989.6 |
| 6te | 13326.4 |
| 7te | 71334.2 |
| 8te | 84078.3 |
Effektive Kernladungen
Die folgenden sind „Clementi-Raimondi“ effektive Kernladungen, Zeff. Folgen Sie den Hyperlinks für weitere Einzelheiten und für Diagramme in verschiedenen Formaten.
| 1s | 7.6579 | ||||||
|---|---|---|---|---|---|---|---|
| 2s | 4.49 | 2p | 4.45 | ||||
| 3s | (keine Daten) | 3p | (keine Daten) | 3d | (keine Daten) | ||
| 4s | (keine Daten) | 4p | (keine Daten) | 4d | (keine Daten) | 4f | (keine Daten) |
| 5s | (keine Daten) | 5p | (keine Daten) | 5d | (keine Daten) | ||
| 6s | (keine Daten) | 6p | (keine Angaben) | ||||
| 7s | |||||||
Diese effektiven Kernladungen, Zeff, sind aus den folgenden Quellen übernommen:
- E. Clementi und D.L.Raimondi, J. Chem. Phys. 1963, 38, 2686.
- E. Clementi, D.L.Raimondi, and W.P. Reinhardt, J. Chem. Phys. 1967, 47, 1300.
Elektronenbindungsenergien
| Label | Orbital | eV |
|---|---|---|
| K | 1s | 543.1 |
| L I | 2s | 41.6 |
Anmerkungen
Ich danke Gwyn Williams (Jefferson Laboratory, Virginia, USA) für die Bereitstellung der Daten zur Elektronenbindungsenergie. Die Daten sind den Referenzen 1-3 entnommen. Sie sind an anderer Stelle im WWW (Referenz 4) und in Papierform (Referenz 5) aufgeführt.
- J. A. Bearden und A. F. Burr, „Reevaluation of X-Ray Atomic Energy Levels“, Rev. Mod. Phys., 1967, 39, 125.
- M. Cardona and L. Ley, Eds., Photoemission in Solids I: General Principles (Springer-Verlag, Berlin) mit zusätzlichen Korrekturen, 1978.
- Gwyn Williams WWW-Wertetabelle
- D.R. Lide, (Ed.) in Chemical Rubber Company handbook of chemistry and physics, CRC Press, Boca Raton, Florida, USA, 81st edition, 2000.
- J. C. Fuggle und N. Mårtensson, „Core-Level Binding Energies in Metals“, J. Electron Spectrosc. Relat. Phenom. 1980, 21, 275.