- Prilosec OTC Produktmonographie
- 1.1 Charakterisierung von häufigem Sodbrennen
- 1.2 Freiverkäufliche Medikamente gegen Sodbrennen
- Beschreibung
- Zusammensetzung
- 3.1 Wirkstoff
- 3.2 Inaktive Bestandteile
- Klinische Pharmakologie
- 4.1 Wirkmechanismus
- 4.2 Hemmung der Magensäuresekretion
- 4.3 Pharmakokinetik
- Klinische Wirksamkeitsstudien
- 5.1 Primäre Wirksamkeitsendpunkte (24 Stunden frei von Sodbrennen)
- 5.2 Ergebnisse der sekundären Wirksamkeitsendpunkte (kein nächtliches Sodbrennen und kein mehr als leichtes Sodbrennen)
- OTC Label Comprehension And Compliance
- 6.1 Compliance Study Results
- Indikation und Anwendung
- Sicherheit
- 8.1 Gegenanzeigen
- 8.2 Wechselwirkungen mit Arzneimitteln
Prilosec OTC Produktmonographie
Hier finden Sie alle Informationen, die Sie benötigen, um Prilosec OTC besser zu verstehen, bevor Sie es Ihren Patienten empfehlen.
Prilosec OTC (Omeprazol 20 mg als Omeprazol-Magnesium 20,6 mg) wurde von der U.S. Food and Drug Administration als rezeptfreies Medikament für die Behandlung von häufigem Sodbrennen zugelassen, definiert als Sodbrennen, das an zwei oder mehr Tagen pro Woche auftritt. Mit Prilosec OTC steht den medizinischen Fachkräften eine rezeptfreie Therapieoption zur Verfügung, die sie erwachsenen Patienten mit häufigen Sodbrennensymptomen empfehlen können.
In der Vergangenheit gehörten zu den Behandlungsoptionen für selbstbehandelnde Verbraucher Antazida und H2-Rezeptor-Antagonisten (H2RA). Jetzt haben die Verbraucher Zugang zu PPIs, einschließlich POTC, einer lang anhaltenden Behandlungsoption zur Kontrolle häufiger Sodbrennensymptome – eine Dosis pro Tag wirkt bis zu 24 Stunden lang im Rahmen einer 14-tägigen Therapie. Dieser Abschnitt gibt einen Überblick über häufiges Sodbrennen und seine Behandlungsgewohnheiten.
1.1 Charakterisierung von häufigem Sodbrennen
Das Sodbrennen wird als ein Gefühl von Unbehagen in der Mitte der Brust beschrieben, das sich bis zum Hals und Nacken ausbreitet, begleitet von einem brennenden oder schmerzhaften Gefühl unter dem Brustbein. Eine Umfrage aus dem Jahr 2003 ergab, dass in den Vereinigten Staaten etwa 65 % der erwachsenen Gesamtbevölkerung von Sodbrennen betroffen sind, wobei etwa 15 Millionen Erwachsene täglich unter Sodbrennen leiden.1a
Etwas mehr Frauen (59 %) als Männer berichten über häufiges Sodbrennen.1a,2 Das Durchschnittsalter eines Verbrauchers mit häufigem Sodbrennen liegt bei 45 bis 50 Jahren,1a und Sodbrennen hat eine leichte Tendenz, mit dem Alter zuzunehmen.2 Geografische Lage, Familienstand, Familienstand (Kinder), Bildungsniveau, Art und Niveau der Beschäftigung und sozioökonomischer Status spielen alle eine Rolle bei der Neigung zu Sodbrennen.3
Abbildung 1 zeigt die Häufigkeit aller Sodbrennen-Episoden in einer 2003 durchgeführten Umfrage unter einer repräsentativen Population von Erwachsenen mit Sodbrennen.1a
Abbildung 1. Häufigkeit von Sodbrennen in der US-amerikanischen Sodbrennenpopulation1a

Verbraucher mit häufigem Sodbrennen gaben an, seit langem unter Sodbrennensymptomen zu leiden.
Die Mehrheit der Verbraucher mit häufigem Sodbrennen hat ihre Symptome mit medizinischem Fachpersonal besprochen. Die meisten Verbraucher mit häufigem Sodbrennen (62 %) haben ihre Symptome ihrem Hausarzt mitgeteilt; 16 % bzw. 2 % haben Gastroenterologen oder Kardiologen aufgesucht; und 30 % haben sich an Apotheker gewandt.1a
1.2 Freiverkäufliche Medikamente gegen Sodbrennen
Die meisten Verbraucher mit häufigem Sodbrennen diagnostizieren und behandeln sich selbst mit frei verkäuflichen Medikamenten. In einer Umfrage aus dem Jahr 2001 gaben etwa 80 % der Personen mit häufigem Sodbrennen an, rezeptfreie Medikamente gegen Sodbrennen zu verwenden.1a
In dieser Studie stuften mehr als 70 % der Personen, die häufig unter Sodbrennen litten, ihre Symptome als mäßig bis schwer ein, und die meisten Personen, die häufig unter Sodbrennen litten, gaben an, bei den ersten Anzeichen von Symptomen Medikamente einzunehmen, um eine Verschlimmerung der Symptome zu verhindern oder sie zu lindern. Im Allgemeinen berichteten Verbraucher mit häufigem Sodbrennen, dass sie ihr Sodbrennen durch die Einnahme von Antazida allein oder in Kombination mit rezeptfreien H2RAs oder verschreibungspflichtigen PPIs in den Griff bekamen.1a
Beschreibung
Prilosec OTC wird in Packungen mit 14, 28 und 42 Tabletten angeboten. Diese Packungsgrößen enthalten eine, zwei bzw. drei 14-tägige Behandlungsreihen. Prilosec OTC ist eine rosafarbene (lachsfarbene) Tablette, die aus mehreren magensaftresistenten Pellets besteht, die 20,6 mg Omeprazol-Magnesium enthalten, was 20 mg Omeprazol entspricht. Der Wirkstoff ist das Magnesiumsalz von Omeprazol, das die Tablettierung ermöglicht. Prilosec OTC ist auch in einer Tablette mit Wildbeer-Geschmack erhältlich, die beim Schlucken der Tablette einen Hauch von Geschmack bietet. Prilosec OTC Wildberry ist nicht zum Kauen oder Lutschen gedacht. Es handelt sich um eine violette Tablette, die in den Größen 14 und 42 ct. erhältlich ist. Derzeit wird diese Tablettenformulierung als rezeptfreies Produkt in Schweden und als verschreibungspflichtiges Produkt in mehr als 30 anderen Ländern vermarktet.1a
Zusammensetzung
3.1 Wirkstoff
Der Wirkstoff in Prilosec OTC Tabletten mit verzögerter Wirkstofffreisetzung ist Omeprazol-Magnesium; seine chemische Bezeichnung ist Di-5-methoxy-2-sulfinyl]-1H-benzimidazol-Magnesium. Omeprazol-Magnesium hat ein Molekulargewicht von 713,1. Seine Strukturformel ist in Abbildung 2.4 dargestellt
Omeprazolmagnesium ist eine kristalline Substanz, die in Methanol leicht und in Wasser schwer löslich ist. Omeprazol-Magnesium dissoziiert schnell in Wasser und bildet Omeprazol und Magnesium.4
Abbildung 2. Chemische Struktur von Omeprazol-Magnesium4

3.2 Inaktive Bestandteile
Prilosec OTC Inaktive Bestandteile: Glycerylmonostearat, Hydroxypropylcellulose, Hypromellose, Eisenoxid, Magnesiumstearat, Methacrylsäure-Copolymer, mikrokristalline Cellulose, Paraffin, Polyethylenglycol 6000, Polysorbat 80, Polyvinylpyrrolidon, Natriumstearylfumarat, Stärke, Saccharose, Talkum, Titandioxid, Triethylcitrat5
Prilosec OTC Wildberry Flavor Inaktive Bestandteile: FD&C blau Nr. 2 Aluminiumsee, FD&C rot Nr. 40 Aluminiumsee, Aroma, Glycerylmonostearat, Hydroxypropylcellulose, Hypromellose, Magnesiumstearat, Methacrylsäure-Copolymer, Glimmer, mikrokristalline Cellulose, Polyethylenglykol 6000, Polysorbat 80, Polyvinylpyrrolidon, Saccharin-Natrium, Natriumstearylfumarat, Stärke, Saccharose, Talkum, Titandioxid, Triethylcitrat
Klinische Pharmakologie
4.1 Wirkmechanismus
Omeprazol gehört zu der Klasse der Arzneimittel, die als substituierte Benzimidazole bekannt sind.6 Omeprazol bindet irreversibel an die Protonenpumpe (H+/K+-ATPase-Enzymsystem) an der sekretorischen Oberfläche der Parietalzelle des Magens.6-8 Die Bindung hemmt oder unterdrückt die Fähigkeit der Parietalzelle, Magensäure zu sezernieren (Abbildung 3).
Abbildung 3. Wirkmechanismus von Omeprazol4

Klinische Pharmakologie
4.2 Hemmung der Magensäuresekretion
Der Rückfluss von Magensäure in die Speiseröhre ist die Hauptursache für die Symptome von Sodbrennen. Omeprazol hemmt sowohl die basale als auch die stimulierte Säuresekretion aus den Parietalzellen, unabhängig vom Stimulus. Nach 24 Stunden ist die Säuresekretion der Parietalzellen des Magens nach einer Einzeldosis auf etwa 50 % der maximalen Menge reduziert. Wenn Omeprazol abgesetzt wird, kehrt die Fähigkeit zur Magensäuresekretion innerhalb weniger Tage allmählich zurück, da neue Protonenpumpen gebildet werden.4
Pharmakodynamische Daten zeigten, dass Omeprazol 20 mg täglich eine ausgeprägte und konsistente Hemmung der Magensäuresekretion über 24 Stunden bewirkt.4 Das Ausmaß und die Konsistenz dieser Wirkung waren bei 20 mg gegenüber 10 mg täglicher Omeprazol-Dosis signifikant besser. Abbildung 4 veranschaulicht die überlegene und konsistentere antisekretorische Wirkung von Omeprazol in einer Dosierung von 20 mg oder höher.9 Sie zeigt auch, dass eine Tagesdosis von 20 mg Omeprazol eine deutlich stärkere und konsistentere Hemmung bewirkt als die niedrigeren Dosen, aber keine vollständige Blockade der Magensäuresekretion über das 24-Stunden-Dosierungsintervall.
Abbildung 4. Hemmende Wirkungen einer einwöchigen Behandlung mit täglichen Omeprazol-Dosen auf die 24-stündige Magensäuresekretion9

4.3 Pharmakokinetik
Bioverfügbarkeit
Eine Studie mit 29 gesunden amerikanischen Probanden zeigte, dass die Bioverfügbarkeit von Omeprazol Probanden zeigte, dass die Bioverfügbarkeit von Prilosec OTC-Tabletten mit derjenigen der im Handel erhältlichen verschreibungspflichtigen 20-mg-Kapseln von Prilosec® (Omeprazol) vergleichbar ist (siehe Abbildung 5).4 Den Probanden wurde das Behandlungsprodukt als morgendliche Einzeldosis unter Nüchternbedingungen verabreicht. Bei der Studie handelte es sich um eine randomisierte, offene Crossover-Studie mit einer fünftägigen Auswaschphase zwischen den Behandlungen. Die Tablettenformulierung wird in Schweden als rezeptfreies Produkt und in mehr als 30 anderen Ländern als verschreibungspflichtiges Produkt vermarktet.1a
Abbildung 5. Mittlere Plasmakonzentration von Omeprazol im Vergleich zur Zeit: Probanden mit auswertbaren pharmakokinetischen Daten (n = 29)4

Absorption, Verteilung und Metabolismus
Da die Pellets, die Omeprazol-Magnesium in Prilosec OTC-Tabletten enthalten, magensaftresistent sind, sollten die Tabletten nicht geteilt werden, da dies die Beschichtung stören würde. Aufgrund des magensaftresistenten Überzugs beginnt die Absorption erst, nachdem die Tabletten in den Zwölffingerdarm gelangt sind. Dies ist wichtig, da der Kontakt mit dem sauren Milieu des Magens vor dem Eintritt in den Blutkreislauf zu einem Abbau des Omeprazol-Moleküls führen würde, der seine endgültige Wirksamkeit einschränken könnte. Sobald sich Omeprazol-Magnesium in dieser nahezu neutralen Umgebung des Zwölffingerdarms auflöst, wandelt sich das Omeprazol-Ion in seine neutrale Form um. Die gleiche Form von Omeprazol steht für die Absorption zur Verfügung, unabhängig davon, ob es als freie Form, Omeprazol, oder als Salz, Omeprazol-Magnesium, verabreicht wird.10 Die Absorption erfolgt schnell, wobei die maximalen Plasmaspiegel (Cmax) von Omeprazol innerhalb von 0,5 bis 3,5 Stunden nach der oralen Verabreichung erreicht werden.4 Bei gesunden erwachsenen Probanden beträgt die Plasmahalbwertszeit (t1/2) 0,5 bis 1,0 Stunden, und die Gesamtkörper-Clearance liegt bei 500 bis 600 mL/min. Die Wirkdauer von Omeprazol beträgt mehr als 24 Stunden nach einer Einzeldosis, da sich die Parietalzellen in etwa drei bis fünf Tagen umwandeln. Die Proteinbindung beträgt etwa 95 %. Die Hemmung der Säuresekretion hängt mit der Fläche unter der Plasmakonzentrations-Zeit-Kurve zusammen, nicht aber mit der tatsächlichen Plasmakonzentration zu einem bestimmten Zeitpunkt.
Omeprazol wird in der Leber durch Cytochrom-P450-Isoenzyme vollständig metabolisiert. Es werden mindestens sechs Metaboliten gebildet, die keine oder nur eine geringe antisekretorische Wirkung haben. Die Omeprazol-Metaboliten werden in erster Linie mit dem Urin und in zweiter Linie mit den Fäkalien ausgeschieden.4
Klinische Wirksamkeitsstudien
Zwei gut kontrollierte klinische Studien mit 3.120 Probanden unterstützen die Verwendung eines aufeinanderfolgenden 14-tägigen Therapieschemas von Omeprazol-Magnesium zur Behandlung von häufigem Sodbrennen. Beide Studien waren multizentrisch, doppelblind, randomisiert, parallel und placebokontrolliert. Jede Studie untersuchte Omeprazol-Magnesium in einer Dosierung von 10 mg und 20 mg an 14 aufeinanderfolgenden Tagen bei Probanden mit Sodbrennen an zwei oder mehr Tagen pro Woche.1a
Die Studien hatten eine einwöchige Placebo-Phase zur Beurteilung der Sodbrennen-Häufigkeit. Die in Frage kommenden Probanden wurden nach dem Zufallsprinzip in eine zweiwöchige doppelblinde Behandlungsphase eingeteilt, in der sie täglich eine Einzeldosis von entweder Omeprazol-Magnesium 10 mg, Omeprazol-Magnesium 20 mg oder Placebo erhielten. Die Probanden nahmen ihre tägliche Dosis des Studienmedikaments jeden Morgen vor dem Frühstück ein.1a
Der primäre Wirksamkeitsendpunkt war „kein Sodbrennen in den vorangegangenen 24 Stunden“ (d. h. völlige Sodbrennenfreiheit für einen ganzen Tag). Die Wirksamkeit wurde nach der ersten Dosis des Medikaments, bei der letzten Dosis und über 14 Tage der Einnahme während der Doppelblindphase bewertet.1a
Eine Reihe von sekundären Wirksamkeitsendpunkten wurde ebenfalls nach der ersten Dosis des Medikaments und den nachfolgenden Dosen untersucht. Dazu gehörten die „vollständige Verhinderung von nächtlichem Sodbrennen“ und das „Auftreten von nicht mehr als leichtem Sodbrennen „1b
5.1 Primäre Wirksamkeitsendpunkte (24 Stunden frei von Sodbrennen)
Beide klinischen Studien zeigten, dass 20 mg Omeprazol-Magnesium am ersten Tag zu einem signifikanten Behandlungseffekt führte. Wie in Abbildung 6 dargestellt, waren fast 50 % der Probanden in den Behandlungsgruppen mit 20 mg Omeprazol-Magnesium einen ganzen Tag lang nach der ersten Dosis frei von Sodbrennen, gegenüber etwa 32 % der Probanden in der Placebogruppe (Abbildung 6).1a
Abbildung 6. Prozentsatz der Probanden, die 24 Stunden lang kein Sodbrennen hatten – Tag 11a
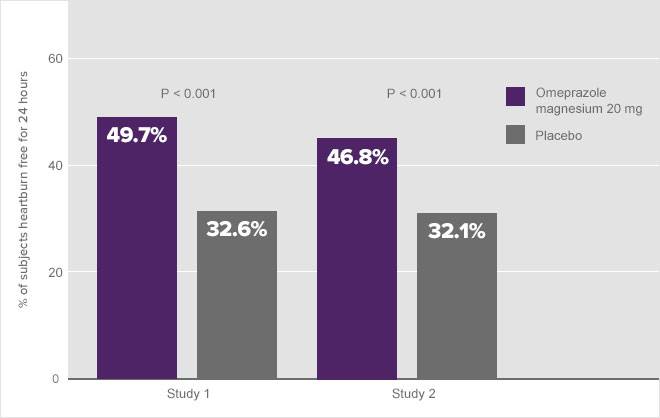
Am Tag 14 lag der Prozentsatz der Probanden, die über eine vollständige Linderung des Sodbrennens berichteten, bei mehr als 70 % (Abbildung 7).1a
Abbildung 7. Prozentsatz der Probanden, die 24 Stunden lang kein Sodbrennen hatten – Zeitverlauf über 14 Tage1a

5.2 Ergebnisse der sekundären Wirksamkeitsendpunkte (kein nächtliches Sodbrennen und kein mehr als leichtes Sodbrennen)
Im Allgemeinen bestätigten die Ergebnisse für diese Endpunkte die Erkenntnisse für die primären Endpunkte.1a
Wenn Probanden mit nur leichtem Sodbrennen zum Wirksamkeitsendpunkt hinzugefügt wurden, berichteten mehr als 80 % derjenigen, die Omeprazol-Magnesium erhielten, über einen signifikanten therapeutischen Nutzen an Tag 1 (Abbildung 8).1a
Abbildung 8. Prozentsatz der Probanden mit höchstens leichtem Sodbrennen – Tag 11a

OTC Label Comprehension And Compliance
6.1 Compliance Study Results
Das Verhalten der Verbraucher und ihr Verständnis für die Anwendung von Prilosec OTC wurden in Studien zum Verständnis des Etiketts und in einer Studie zur tatsächlichen Anwendung untersucht. Dieses Studienprogramm untersuchte die Einhaltung der Anweisungen auf dem Etikett und die Verwendung des Produkts in einem unbeaufsichtigten Umfeld. Im Einzelnen wurde das Programm entwickelt, um festzustellen, ob die Verbraucher Folgendes verstanden haben: 1) die Bevölkerungsgruppe, für die Prilosec OTC am besten geeignet ist (Selbstselektion auf der Grundlage der Häufigkeit des Sodbrennens und des Verständnisses der Warnhinweise auf dem Etikett); 2) wann und wie Prilosec OTC einzunehmen ist (eine Tablette pro Tag an 14 aufeinanderfolgenden Tagen); und 3) wann ein Arzt aufzusuchen ist (als Reaktion auf bestimmte Warnhinweise oder bei erneutem häufigem Sodbrennen). In der Studie zur tatsächlichen Anwendung wurde die Befolgung der Anweisungen auf dem Etikett unter den Bedingungen der tatsächlichen Anwendung ermittelt.1a
-
Für jedes der Selbstselektionskriterien lag die angemessene Wahl in der gesamten Population bei über 90 %.
1a
-
Die Probanden, die sich für die Anwendung des Produkts entschieden, hielten sich in hohem Maße an die Dosierungsanweisungen auf dem Etikett, wobei mehr als 91 % der Probanden das Produkt wie auf dem Etikett angegeben verwendeten, indem sie nicht mehr als eine Tablette pro Dosis und nicht mehr als eine Tablette pro Tag einnahmen.
1a
-
Bei einer dreimonatigen Nachbefragung zeigten die Verbraucher, bei denen die Symptome des Sodbrennens wieder auftraten, weiterhin ein Verhalten, das mit den Anwendungshinweisen auf dem Etikett übereinstimmte.
1a
Die Ergebnisse dieser Studien unterstützen nachdrücklich die angemessene Verwendung von Prilosec OTC durch Verbraucher mit häufigem Sodbrennen und die Fähigkeit der Verbraucher, das Produkt innerhalb der vorgeschlagenen OTC-Etikettangaben korrekt zu verwenden (Abbildung 9).1a
Abbildung 9. Einhaltung der Dosierungsanleitung1a
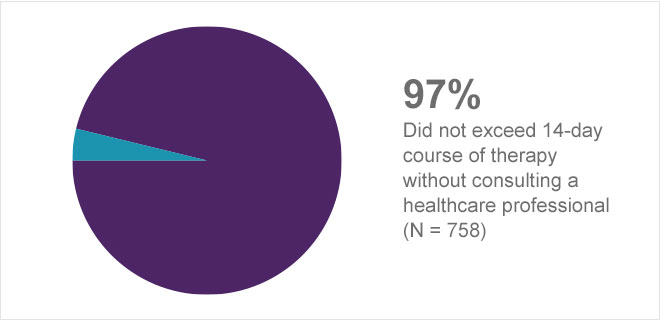
Indikation und Anwendung
Prilosec OTC 20 mg Tabletten sind indiziert für die Behandlung von häufigem Sodbrennen, das definiert ist als Sodbrennen, das an zwei oder mehr Tagen pro Woche auftritt. Die Packungsbeilage von Prilosec OTC enthält folgende Hinweise für die angemessene Anwendung durch Verbraucher mit häufigem Sodbrennen5:

-
Eine Tablette pro Tag behandelt häufiges Sodbrennen für 24 Stunden als Teil einer 14-tägigen Therapie.
-
Die QD-Dosierung minimiert die Unannehmlichkeiten und fördert die Compliance.
-
Ein 14-tägiges Dosierungsschema zur Behandlung von häufigem Sodbrennen anwenden.
-
Die Gebrauchsinformation empfiehlt dem Verbraucher, einen Arzt aufzusuchen.
-
Verbrauchern wird empfohlen, nicht mehr als eine 14-tägige Kur alle vier Monate einzunehmen, es sei denn, ein Arzt hat etwas anderes verordnet.
Sicherheit
8.1 Gegenanzeigen
Prilosec OTC ist kontraindiziert für Personen, die überempfindlich gegen Omeprazol sind. Verbraucher, die an bestimmten Erkrankungen und/oder Symptomen leiden, werden auf dem Etikett angewiesen, das Produkt entweder nicht zu verwenden oder einen Arzt zu konsultieren.5
8.2 Wechselwirkungen mit Arzneimitteln
Die möglichen metabolischen Wechselwirkungen mit Omeprazol (das hauptsächlich durch das hepatische Cytochrom-P450-Isoenzym CYP2C19 metabolisiert wird) wurden systematisch untersucht, insbesondere in Bezug auf Warfarin, Diazepam, Digoxin und Clopidogrel.4
FDA Health Advisory Issued
Erfahren Sie, warum die Daten empfehlen, die Kombination von Prilosec OTC (Omeprazol) und Plavix® (Clopidogrel) zu vermeiden.
Während klinisch bedeutsame Wechselwirkungen zwischen Warfarin oder Digoxin und Omeprazol unwahrscheinlich sind, führte das engere therapeutische Fenster für diese Medikamente zu der konservativen Vorsichtsmaßnahme, sie auf dem Etikett für Prilosec OTC aufzuführen.4
Darüber hinaus hat die FDA eine Kennzeichnung gefordert, die Patienten vor der Einnahme von POTC warnt, wenn sie einnehmen:
Cilostizol, verschreibungspflichtige Antimykotika oder Mittel gegen Hefepilze, Diazepam, Digoxin, Tacroimus, Mycophenolat Mofetil, verschreibungspflichtige antoretrovirale Medikamente und Methotrexat.
Warfarin
Bei Patienten, die gleichzeitig Warfarin und Omeprazol einnehmen, wurden nach dem Inverkehrbringen Veränderungen der Prothrombinwerte berichtet. Erhöhungen der INR und der Prothrombinzeit können zu abnormalen Blutungen und sogar zum Tod führen. Patienten, die gleichzeitig mit PPIs und Warfarin behandelt werden, müssen möglicherweise auf Erhöhungen der INR und der Prothrombinzeit überwacht werden.
Diazepam
Die gleichzeitige Verabreichung mit Diazepam wurde ebenfalls im Abschnitt „Warnhinweise“ aufgeführt, weil Omeprazol die Diazepam-Clearance signifikant reduziert, obwohl es aufgrund des relativ breiten therapeutischen Fensters für Diazepam unwahrscheinlich ist, dass dieser Effekt von Omeprazol klinisch signifikant ist.4
Antiretrovirale Wirkstoffe
Es wurde berichtet, dass die gleichzeitige Verabreichung von Omeprazol die Plasmaspiegel antiretroviraler Wirkstoffe beeinflussen kann, daher wird eine angemessene klinische Überwachung empfohlen.
Methotrexat
Daten scheinen darauf hinzuweisen, dass die Wechselwirkung zwischen Omeprazol und Methotrexat mit einer verminderten Ausscheidung von Methotrexat verbunden sein kann, was zu einer Methotrexat-Toxizität führt. Die zugelassene Kennzeichnung für verschreibungspflichtige Methotrexat-Produkte und alle PPI-Verschreibungsetiketten enthalten diese Informationen.
Tacrolimus
Die gleichzeitige Verabreichung von Omeprazol und Tacrolimus kann die Serumspiegel von Tacrolimus erhöhen.
Arzneimittel mit pH-abhängiger Absorption
Wie bei anderen PPIs und H2RAs erhöht Omeprazol den intragastrischen pH-Wert (verringert den Säuregehalt), was die Absorption von Arzneimitteln mit pH-abhängiger Absorption beeinträchtigen kann, z. B., Ketoconazol, Itraconazol oder Mycophenolatmofetil. In einer Studie wurde nachgewiesen, dass die Absorption von Ketoconazol nach Verabreichung von Omeprazol stark vermindert war. Ebenso zeigte eine andere Studie, dass die Itraconazol-Resorption vermindert war, wenn es nach einer zweiwöchigen Omeprazol-Kur verabreicht wurde.4
Die gleichzeitige Verabreichung von Mycophenolatmofetil mit einem PPI führt nach den in der Literatur zitierten Studien zu einer verringerten systemischen Exposition von Mycophenolatmofetil.11 Dieser Effekt ist möglicherweise auf die Unterdrückung der Magensäure durch den PPI zurückzuführen, was zu einer unvollständigen Auflösung von Mycophenolatmofetil und einer anschließenden schlechten Resorption führen kann. Diese Information ist in den aktuellen Etiketten von Mycophenolatmofetil enthalten.
Daher werden auf dem Etikett von Prilosec OTC mögliche Wechselwirkungen mit diesen Arzneimitteln unter dem Abschnitt „Warnhinweise“ der Arzneimittelinformationen aufgeführt.5
Besondere Bevölkerungsgruppen
Verwendung in der Schwangerschaft und Stillzeit: Die Packungsbeilage von Prilosec OTC weist schwangere oder stillende Frauen darauf hin, vor der Anwendung einen Arzt zu konsultieren.5
Verwendung bei Kindern: Prilosec OTC ist für die Behandlung von häufigem Sodbrennen bei Kindern ab 18 Jahren angezeigt. Bei Kindern unter 18 Jahren mit häufigem Sodbrennen wird auf dem Etikett empfohlen, vor der Anwendung einen Arzt zu konsultieren.5
Nebenwirkungen
Ärzte haben Omeprazol Millionen von Patienten verschrieben, um säurebedingte Beschwerden sicher zu behandeln.7
Die Sicherheit von Omeprazol wurde in 15 neuen klinischen Studien mit Omeprazol-Magnesium (n > 18.000) bestätigt. Die häufigsten unerwünschten Wirkungen waren Kopfschmerzen und Durchfall, die mit denen in den klinischen Studien und der Überwachung nach der Markteinführung von verschreibungspflichtigem Prilosec übereinstimmen. Prilosec OTC hatte ein ähnliches Verträglichkeitsprofil wie Placebo.1a
Verfügbarkeit und Lagerung
Prilosec OTC-Tabletten in einer Dosierung von 20 mg werden in Blisterpackungen geliefert. Prilosec OTC ist rezeptfrei in drei verschiedenen Größen erhältlich 5:
-
Packung mit 14 Tabletten (eine 14-tägige Behandlung)
-
Packung mit 28 Tabletten (zwei 14-tägige Behandlungen)
-
Packung mit 42 Tabletten (drei 14-tägige Behandlungen)
Prilosec OTC Wildberry Flavor Tabletten in einer Dosierung von 20 mg sind in Blisterpackungen erhältlich. Prilosec OTC Wildberry Flavor ist rezeptfrei in zwei verschiedenen Größen erhältlich5:
-
Packung mit 14 Tabletten (eine 14-tägige Behandlung)
-
Packung mit 42 Tabletten (drei 14-tägige Behandlungen)
Lagerungsbedingungen
-
Lagerung bei 20°C bis 25°C (68°F bis 77°F). 5
-
Vor Feuchtigkeit schützen. 5
1a Daten in den Akten. Procter & Gamble.
1b Vergleich von Prilosec OTC™ (Omeprazol-Magnesium 20,6 mg) mit Placebo für 14 Tage bei der Behandlung von häufigem Sodbrennen. Zeitschrift für klinische Pharmazie und Therapeutik. 2005;30:105-112.
2 Oliveria SA, Christos PJ, Talley NJ, et al. Heartburn risk factors, knowledge, and prevention strategies: a population-based survey of individuals with heartburn. Arch Intern Med. 1999;159:1592-1598.
3 Profil der bedürftigen Verbraucher. Wenn der Süden wieder aufsteigt, ist es wahrscheinlich nur Gas: ein unbeschwerter Blick auf schwere Mägen. Progressive Grocer 1995;98-99.
sup>4 Daten in den Akten. AstraZeneca LP.
5 Prilosec OTC . Cincinnati, Ohio: Procter & Gamble; 2015.
6 Massoomi F, Savage J, Destache CJ. Omeprazol: eine umfassende Überprüfung. Pharmacotherapy 1993;13:46-59.
7 Prilosec . Wilmington, Del: AstraZeneca LP; 2015.
8 Lindberg P, Brändström A, Wallmark B, et al. Omeprazole: the first proton pump inhibitor. Med Res Rev. 1990;10:1-54.
9 Lind T, Cederberg C, Axelson M, et al. Long-term acid inhibitory effect of different daily doses of omeprazole 24 hours after dosing. Scand J Gastroenterol. 1986;21(suppl 118):137-138.
10 Losec . Auckland, New Zealand: AstraZeneca Limited; 2015.
11The role of proton pump inhibitors on early mycophenolic acid exposure in kidney transplantation: evidence from the CLEAR study. Kiberd BA, Wrobel M, Danavino R, et al. Ther Drug Monit. 2011 Feb; 33(1):120-3; Protonenpumpenhemmer reduzieren die Mycophenolat-Exposition bei Herztransplantationsempfängern – eine prospektive, kontrollierte Fallstudie. Kofler S, Shvets N, Bigdeli AK, et al. Amer J. Transplant. 2009 Jul; 9(7):1650-6. Epub 2009 June 10.