Erregungs-Kontraktions-Kopplung
Die Erregungs-Kontraktions-Kopplung ist das Bindeglied (Transduktion) zwischen dem im Sarkolemm erzeugten Aktionspotential und dem Beginn einer Muskelkontraktion. Der Auslöser für die Kalziumfreisetzung aus dem sarkoplasmatischen Retikulum in das Sarkoplasma ist ein neuronales Signal. Jede Skelettmuskelfaser wird von einem Motoneuron gesteuert, das Signale aus dem Gehirn oder dem Rückenmark an den Muskel weiterleitet. Der Bereich des Sarkolemmas auf der Muskelfaser, der mit dem Neuron interagiert, wird als motorische Endplatte bezeichnet. Das Ende des Axons des Neurons wird als synaptisches Terminal bezeichnet und hat keinen Kontakt mit der motorischen Endplatte. Ein kleiner Raum, der synaptische Spalt, trennt das synaptische Terminal von der motorischen Endplatte. Elektrische Signale wandern entlang des Axons des Neurons, das sich durch den Muskel verzweigt und an einer neuromuskulären Verbindung mit einzelnen Muskelfasern verbunden ist.
Die Fähigkeit von Zellen, elektrisch zu kommunizieren, erfordert, dass die Zellen Energie aufwenden, um ein elektrisches Gefälle über ihre Zellmembranen zu erzeugen. Dieses Ladungsgefälle wird von Ionen getragen, die unterschiedlich über die Membran verteilt sind. Jedes Ion übt einen elektrischen Einfluss und einen Konzentrationseinfluss aus. So wie sich Milch mit Kaffee vermischt, ohne dass man umrühren muss, verteilen sich auch die Ionen gleichmäßig, wenn man sie lässt. In diesem Fall ist es ihnen nicht gestattet, in einen gleichmäßig gemischten Zustand zurückzukehren.
Die Natrium-Kalium-ATPase verwendet zelluläre Energie, um K+-Ionen innerhalb der Zelle und Na+-Ionen außerhalb zu bewegen. Dadurch entsteht nur eine geringe elektrische Ladung, aber ein großes Konzentrationsgefälle. In der Zelle befindet sich viel K+ und außerhalb der Zelle viel Na+. Kalium kann die Zelle durch K+-Kanäle verlassen, die zu 90 % der Zeit geöffnet sind, und das tut es auch. Die Na+-Kanäle sind jedoch nur selten geöffnet, so dass Na+ außerhalb der Zelle verbleibt. Wenn K+ die Zelle aufgrund des Konzentrationsgradienten verlässt, bleibt eine negative Ladung zurück. In Ruhe besteht also ein großer Konzentrationsgradient für Na+, das in die Zelle eintritt, und es kommt zu einer Anhäufung negativer Ladungen, die in der Zelle zurückbleiben. Dies ist das Ruhemembranpotenzial. Das Potenzial bedeutet in diesem Zusammenhang eine Trennung der elektrischen Ladung, die in der Lage ist, Arbeit zu verrichten. Es wird in Volt gemessen, genau wie eine Batterie. Das Transmembranpotenzial ist jedoch wesentlich kleiner (0,07 V); daher wird der kleine Wert in Millivolt (mV) oder 70 mV angegeben. Da das Innere einer Zelle im Vergleich zum Äußeren negativ ist, bedeutet ein Minuszeichen den Überschuss an negativen Ladungen im Inneren der Zelle, also -70 mV.
Wenn ein Ereignis die Durchlässigkeit der Membran für Na+-Ionen verändert, gelangen diese in die Zelle. Dadurch ändert sich die Spannung. Dies ist ein elektrisches Ereignis, das als Aktionspotential bezeichnet wird und als zelluläres Signal verwendet werden kann. Die Kommunikation zwischen Nerven und Muskeln erfolgt über Neurotransmitter. Aktionspotenziale von Neuronen bewirken die Freisetzung von Neurotransmittern aus dem synaptischen Terminal in den synaptischen Spalt, wo sie dann durch den synaptischen Spalt diffundieren und an ein Rezeptormolekül auf der motorischen Endplatte binden können. Die motorische Endplatte verfügt über junktionale Falten – Falten im Sarkolemm, die eine große Oberfläche für die Bindung des Neurotransmitters an die Rezeptoren schaffen. Die Rezeptoren sind eigentlich Natriumkanäle, die sich öffnen, um den Durchgang von Na+ in die Zelle zu ermöglichen, wenn sie ein Neurotransmittersignal erhalten.
Acetylcholin (ACh) ist ein Neurotransmitter, der von Motoneuronen freigesetzt wird und sich an Rezeptoren in der motorischen Endplatte bindet. Die Freisetzung des Neurotransmitters erfolgt, wenn ein Aktionspotenzial das Axon des Motoneurons hinunterwandert, was zu einer veränderten Permeabilität der synaptischen Terminalmembran und einem Kalziumeinstrom führt. Die Ca2+-Ionen ermöglichen es den synaptischen Vesikeln, sich zur präsynaptischen Membran (auf dem Neuron) zu bewegen und sich mit ihr zu verbinden, wodurch Neurotransmitter aus den Vesikeln in den synaptischen Spalt freigesetzt werden. Sobald ACh vom synaptischen Terminal freigesetzt wird, diffundiert es durch den synaptischen Spalt zur motorischen Endplatte, wo es an ACh-Rezeptoren bindet. Wenn ein Neurotransmitter bindet, öffnen sich diese Ionenkanäle, und Na+-Ionen durchqueren die Membran in die Muskelzelle. Dadurch wird der Spannungsunterschied zwischen dem Inneren und dem Äußeren der Zelle verringert, was als Depolarisation bezeichnet wird. Da ACh an der motorischen Endplatte bindet, wird diese Depolarisation als Endplattenpotenzial bezeichnet. Die Depolarisation breitet sich dann entlang des Sarkolemmas aus und erzeugt ein Aktionspotenzial, da Natriumkanäle in der Nähe der ursprünglichen Depolarisationsstelle die Spannungsänderung erkennen und sich öffnen. Das Aktionspotenzial bewegt sich durch die gesamte Zelle und erzeugt eine Welle der Depolarisation.
ACh wird durch das Enzym Acetylcholinesterase (AChE) in Acetyl und Cholin gespalten. AChE befindet sich im synaptischen Spalt und baut ACh ab, damit es nicht an ACh-Rezeptoren gebunden bleibt, was eine unerwünschte verlängerte Muskelkontraktion verursachen würde (Abbildung 6.9).
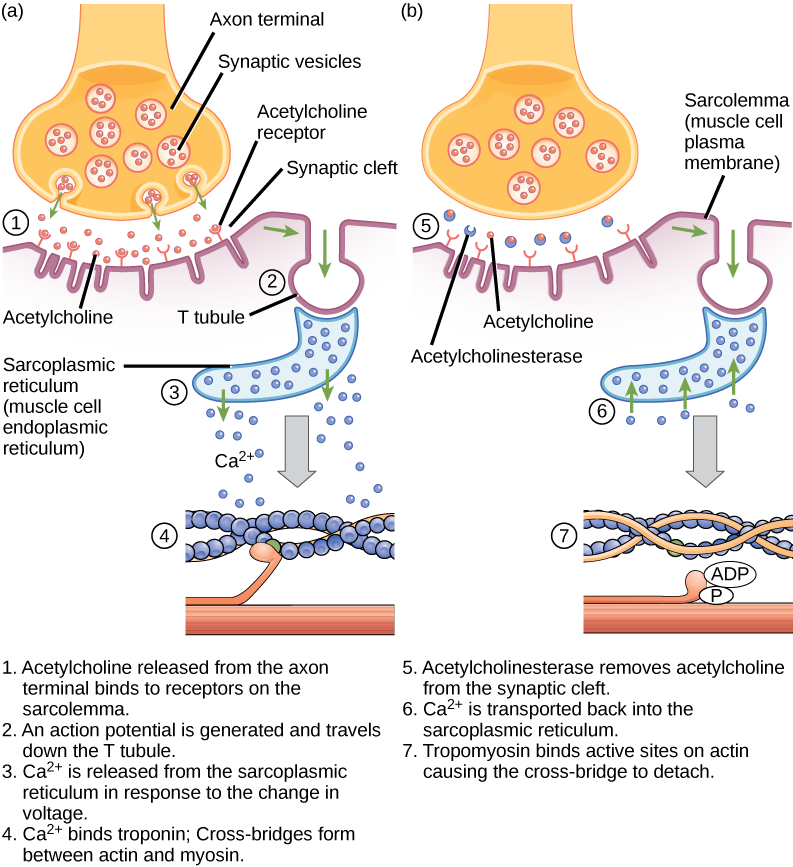
Abbildung 6.9. Dieses Diagramm zeigt die Erregungs-Kontraktions-Kopplung bei einer Skelettmuskelkontraktion. Das sarkoplasmatische Retikulum ist ein spezialisiertes endoplasmatisches Retikulum, das in Muskelzellen zu finden ist.
Bewegung \(\PageIndex{1}\)
Das tödliche Nervengas Sarin hemmt irreversibel die Acetylcholinesterase. Wie wirkt sich Sarin auf die Muskelkontraktion aus?
Nach einer Depolarisation kehrt die Membran in ihren Ruhezustand zurück. Dies wird als Repolarisation bezeichnet, bei der sich spannungsgesteuerte Natriumkanäle schließen. Die Kaliumkanäle haben weiterhin einen Leitwert von 90 %. Da die Natrium-Kalium-ATPase der Plasmamembran stets Ionen transportiert, wird der Ruhezustand (innen negativ geladen im Vergleich zu außen) wiederhergestellt. Der Zeitraum unmittelbar nach der Übertragung eines Impulses in einem Nerv oder Muskel, in dem ein Neuron oder eine Muskelzelle wieder in der Lage ist, einen weiteren Impuls zu übertragen, wird als Refraktärzeit bezeichnet. Während der Refraktärzeit kann die Membran kein weiteres Aktionspotenzial erzeugen. Die Refraktärzeit ermöglicht es den spannungsempfindlichen Ionenkanälen, in ihre Ruhekonfiguration zurückzukehren. Die Natrium-Kalium-ATPase bewegt kontinuierlich Na+ aus der Zelle heraus und K+ zurück in die Zelle, und das K+ entweicht unter Zurücklassung negativer Ladung. Sehr schnell repolarisiert sich die Membran, so dass sie wieder depolarisiert werden kann.