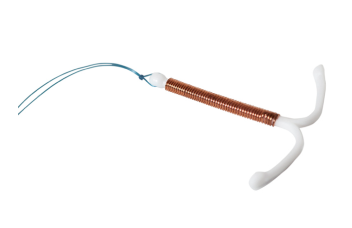
Um estudo clínico conduzido por pesquisadores das Universidades de Birmingham e Nottingham revelou que o dispositivo intra-uterino Mirena (DIU) tratou os ciclos menstruais pesados melhor do que outras opções médicas convencionais. O estudo, denominado estudo ECLIPSE, foi publicado na edição de dezembro de 2012 do New England Journal of Medicine.
O estudo envolveu 571 mulheres que consultaram clínicos gerais sobre períodos pesados, uma condição conhecida como menorragia. Um grande número de mulheres sofre de menorragia, e foi responsável por 20% de todas as consultas ginecológicas no Reino Unido. Nos Estados Unidos, 10 milhões de mulheres são afectadas pela menorragia. Embora Mirena tenha se mostrado eficaz no tratamento de períodos pesados, ainda tem um risco de efeitos colaterais.
Mais Mulheres Preferiram Mirena
As participantes do estudo concordaram em ser atribuídas aleatoriamente vários tratamentos para períodos pesados, incluindo Mirena ou ácido mefenâmico e ácido tranexâmico combinados com combinações variáveis de estrogênio e progestógeno. Os cientistas mediram fatores como experiência individual do paciente, dificuldades práticas com o trabalho, vida social e familiar e saúde física e mental em geral durante um período de dois anos.
Após dois anos, as mulheres que usaram Mirena tinham aproximadamente duas vezes mais probabilidade de ainda estar usando o DIU do que aquelas que estavam tomando outros medicamentos, e 49% das mulheres do estudo que não foram inicialmente designadas para o DIU mudaram para ele. Segundo as participantes, os outros tratamentos não foram eficazes.
Um dos autores do estudo, Janesh Gupta, professora de Obstetrícia e Ginecologia da Universidade de Birmingham, disse: “Este ensaio deve encorajar o uso de DIUs nos cuidados primários. Este estudo mostra que o LNG-IUS (Mirena) é a primeira escolha mais eficaz, como avaliado pelo impacto do sangramento na qualidade de vida das mulheres”
Os médicos do estudo também apontaram que muitas mulheres que têm sangramento menstrual pesado não procuram ajuda, e um objetivo é educar as mulheres sobre as opções de tratamento.
Nos Estados Unidos, Mirena é uma opção atraente de controle de natalidade para mulheres que têm pelo menos um filho e estão procurando um controle de natalidade conveniente e de longo prazo. Sob o Affordable Care Act, a maioria dos planos de seguro oferecem Mirena e outras opções contraceptivas sem custo para a paciente.
O fabricante da Mirena, Bayer, lançou recentemente um novo DIU hormonal chamado Skyla. Ao contrário da Mirena, o novo DIU destina-se ao uso por mulheres que ainda não tiveram filhos e é eficaz por 3 anos, dois anos menos que a Mirena.
A FDA primeiro aprovou a Mirena em 2000 e depois em 2009 para tratar períodos pesados em mulheres que já usam o DIU contraceptivo. Embora, em um editorial que acompanha o estudo ECLIPSE, a Dra. Eve Espey da Universidade do Novo México diz: “Os dados do apoio ampliando sua aprovação para incluir a menorragia em geral, seja ou não necessária contracepção”
Efeitos colaterais de Mirena levam a processos judiciais
Estes estudos e outros realizados sobre Mirena mostraram que o DIU é conveniente e eficaz na prevenção da gravidez e no tratamento de períodos pesados. Infelizmente, Mirena também demonstrou ter uma série de efeitos colaterais, alguns graves.
A Food and Drug Administration (FDA) recebeu mais de 45.000 relatos de eventos adversos relacionados a Mirena. Um dos efeitos colaterais mais perigosos é o potencial para o DIU migrar para fora do útero. O deslocamento do dispositivo ocorreu em mais de 5.000 casos, e o dispositivo migrou para fora do útero em quase 1.500 casos, levando à hospitalização e cirurgia em alguns casos.
Perfuração do útero ocorreu em vários usuários de Mirena, e essas mulheres estão agora entrando com processos judiciais alegando que a Bayer não as avisou dos efeitos colaterais e que o produto é defeituoso. Especialistas legais estimam que mais centenas de casos podem se seguir.
A Bayer solicitou a consolidação dos casos no Supremo Tribunal de Nova Jersey, mas o pedido foi negado em janeiro.