Objetivos de aprendizaje
- Identificar y nombrar alcanos simples (de cadena recta) dadas las fórmulas y escribir fórmulas para alcanos de cadena recta dados sus nombres.
Comenzamos nuestro estudio de la química orgánica con los hidrocarburos, los compuestos orgánicos más simples, que están formados únicamente por átomos de carbono e hidrógeno. Como hemos señalado, hay varios tipos de hidrocarburos. Se distinguen por los tipos de enlace entre los átomos de carbono y las propiedades que resultan de ese enlace. Los hidrocarburos que sólo tienen enlaces simples carbono-carbono (C-C) y que existen como una cadena continua de átomos de carbono también unidos a átomos de hidrógeno se denominan alcanos (o hidrocarburos saturados). Saturado, en este caso, significa que cada átomo de carbono está unido a otros cuatro átomos (de hidrógeno o de carbono), el máximo posible; no hay dobles ni triples enlaces en las moléculas.
La palabra saturado tiene el mismo significado para los hidrocarburos que para las grasas y aceites alimentarios: la molécula no tiene dobles enlaces carbono-carbono (C=C).
Anteriormente presentamos los tres alcanos más simples: metano (CH4), etano (C2H6) y propano (C3H8), y se muestran de nuevo en la Figura \(\PageIndex{1}).
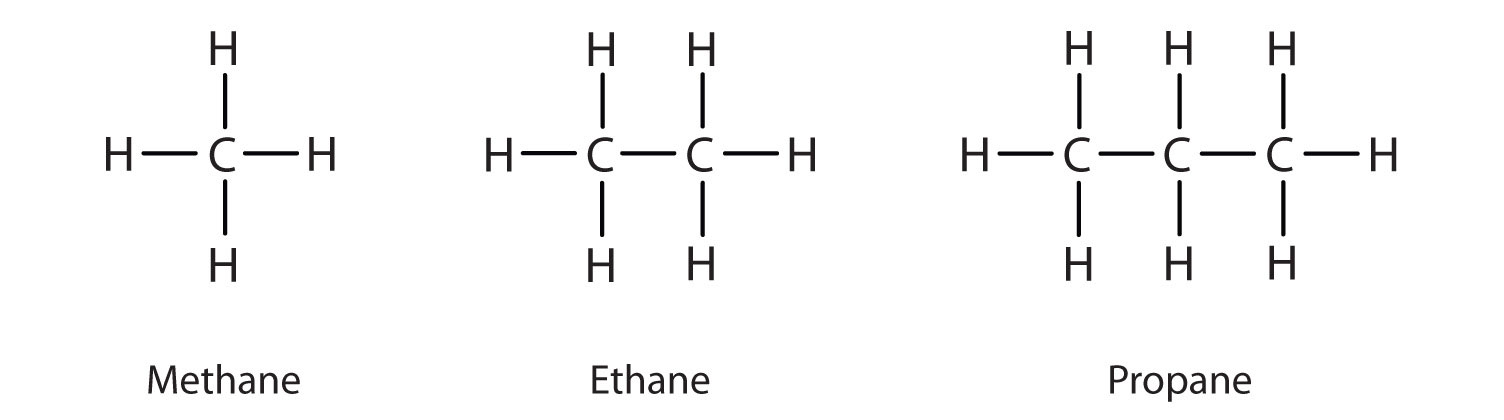
Las representaciones planas que se muestran no representan con exactitud los ángulos de enlace o la geometría molecular. El metano tiene una forma tetraédrica que los químicos suelen representar con cuñas que indican los enlaces que salen hacia ti y líneas discontinuas que indican los enlaces que se alejan de ti. Una línea sólida ordinaria indica un enlace en el plano de la página. Recordemos que la teoría VSEPR predice correctamente una forma tetraédrica para la molécula de metano (Figura \(\PageIndex{2}\)).
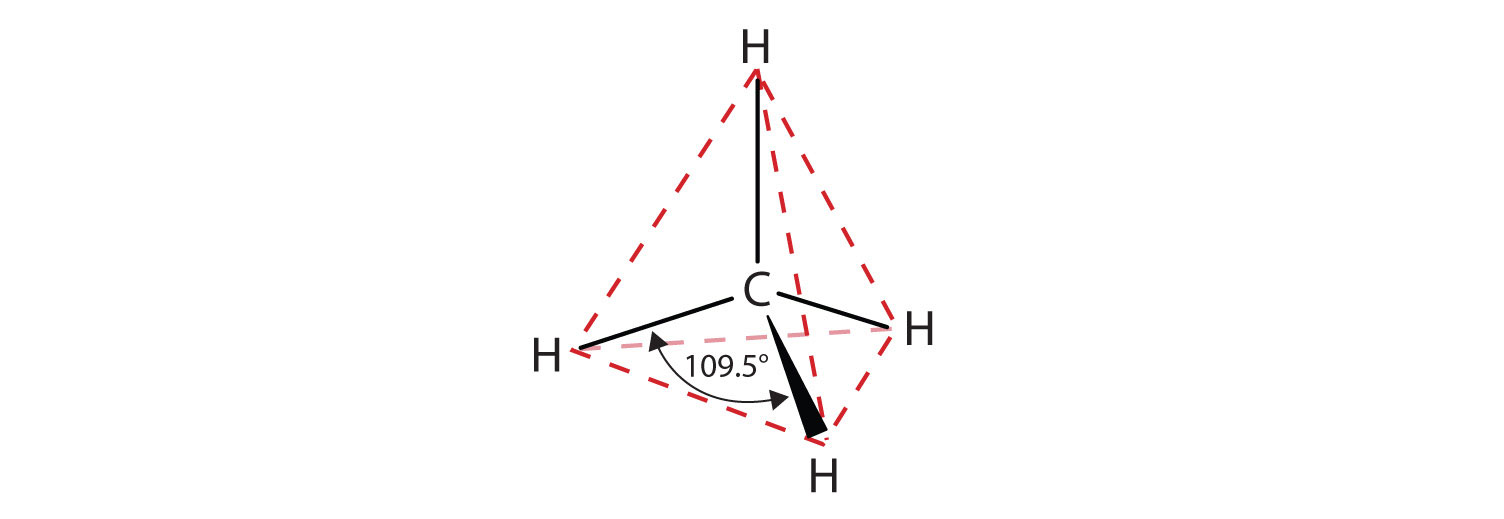
El metano (CH4), el etano (C2H6) y el propano (C3H8) son el principio de una serie de compuestos en los que dos miembros cualesquiera de una secuencia difieren en un átomo de carbono y dos átomos de hidrógeno, es decir, una unidad CH2. Los 10 primeros miembros de esta serie se dan en la Tabla \(\PageIndex{1}).
| Nombre | Fórmula molecular (CnH2n + 2) | Fórmula estructural condensada | Número de posibles isómeros |
|---|---|---|---|
| metano | CH4 | CH4 | – |
| etano | C2H6 | CH3CH3 | – |
| propano | C3H8 | CH3CH2CH3 | – |
| butano | C4H10 | CH3CH2CH2CH3 | 2 |
| pentano | C5H12 | CH3CH2CH2CH3 | 3 |
| hexano | C6H14 | CH3CH2CH2CH3 | 5 |
| heptano | C7H16 | CH3CH2CH2CH2CH3 | 9 |
| octano | C8H18 | CH3CH2CH2CH2CH2CH2CH3 | 18 |
| nonano | C9H20 | CH3CH2CH2CH2CH2CH2CH2CH3 | 35 |
| decano | C10H22 | CH3CH2CH2CH2CH2CH2CH3 | 75 |
Considere la serie de la Figura \(\PageIndex{3}\). La secuencia comienza con C3H8, y se añade una unidad de CH2 en cada paso de la serie. Cualquier familia de compuestos en la que los miembros adyacentes difieren entre sí por un factor definido (en este caso un grupo CH2) se denomina serie homóloga. Los miembros de dicha serie, llamados homólogos, tienen propiedades que varían de forma regular y predecible. El principio de la homología da organización a la química orgánica del mismo modo que la tabla periódica da organización a la química inorgánica. En lugar de un desconcertante conjunto de compuestos de carbono individuales, podemos estudiar unos pocos miembros de una serie homóloga y, a partir de ellos, deducir algunas de las propiedades de otros compuestos de la serie.
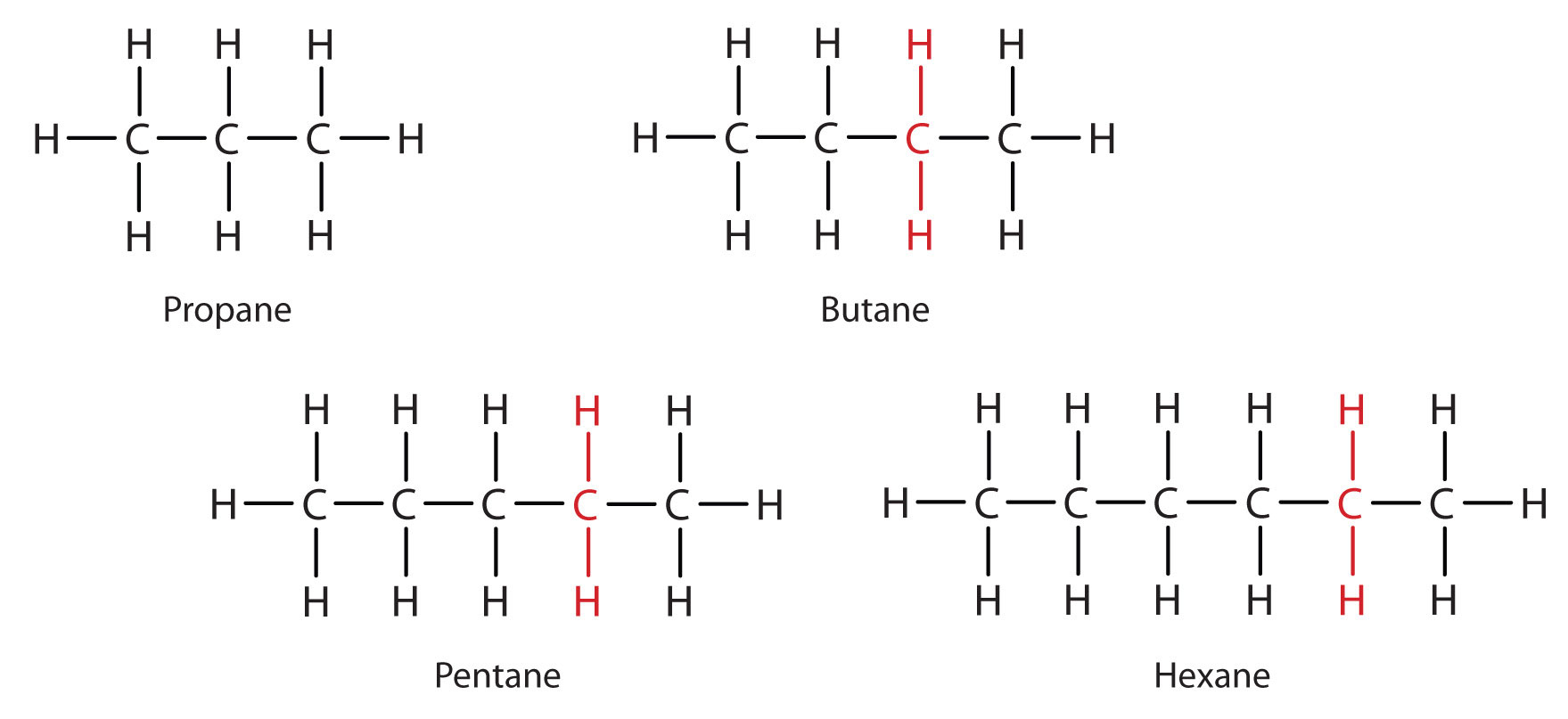
El principio de homología nos permite escribir una fórmula general para los alcanos: CnH2n + 2. Utilizando esta fórmula, podemos escribir una fórmula molecular para cualquier alcano con un número determinado de átomos de carbono. Por ejemplo, un alcano con ocho átomos de carbono tiene la fórmula molecular C8H(2 × 8) + 2 = C8H18.
Lo más importante
- Los alcanos simples existen como una serie homóloga, en la que los miembros adyacentes se diferencian por una unidad CH2.