INLEIDING:
Organische scheikunde is een chemische tak die zich bezighoudt met koolstofverbindingen en met name koolstofverbindingen die in levende wezens voorkomen. Deze tak van de scheikunde was oorspronkelijk beperkt tot verbindingen die door levende organismen worden voortgebracht, maar is uitgebreid met door de mens vervaardigde stoffen zoals polymeren. Polymeren zijn stoffen met een moleculaire structuur die hoofdzakelijk of geheel bestaat uit een groot aantal verwante eenheden, zoals Nylon. Nylon is de meest nuttige synthetische stof met toepassingen die variëren van alledaagse tot industriële processen. Het is een kunststof voor het maken van voorzieningen die tot vezels kunnen worden getrokken of tot alledaagse producten kunnen worden gevouwen. Het wordt gebruikt om plastic machinecomponenten te maken omdat het kosteneffectief en duurzaam is. Het wordt vaak gebruikt voor zijn niet-geleidbaarheid en hittebestendigheid in de elektronica-industrie.
NYLONCHEMISCHESTRUCTUUR:
Nylon is een van de meest gebruikte polymeren als vezel. Nylon heeft geweldige vislijn- en trimmerdraadkenmerken, plus het wordt gebruikt voor sommige “plastic” schroeven en push-in connectoren. Vanwege de kenmerkende amidegroepen in de ruggengraatketen worden nylons ook polyamiden genoemd. Eiwitten, zoals de vervanger van zijde-nylon, zijn ook polyamiden. Deze amidegroepen zijn zeer polair en kunnen zich met elkaar verbinden in termen van waterstof. Om deze reden, en omdat de ruggengraat van nylon zo regelmatig en symmetrisch is. De chemische structuur is weergegeven in figuur 1. Waterstofbinding is de belangrijkste intermoleculaire kracht in nylon. De waterstofatomen met een stikstofverbinding van de ene nylonketen vormen een zeer sterke waterstofverbinding met de carbonylzuurstofatomen van een andere nylonketen. Deze waterstofbruggen produceren zeer krachtige nylonkristallen omdat ze de nylonketens zeer stevig bij elkaar houden.
 Figuur 1: chemischestructuurvanNylon
Figuur 1: chemischestructuurvanNylon
Door: (Yurtoğlu, 2018)
CHEMISCHEREACTIESINVOLLEIDING:
Nylon ontstaat wanneer in een condensatiepolymerisatiereactie de geschikte monomeren (de chemische bouwstenen waaruit polymeren zijn opgebouwd) worden samengevoegd tot een lange keten. Nylon 6-6 monomeren zijn adipinezuur en diaminehexamethyleen, dit is weergegeven in figuur 2. Om het polymeer te maken, worden de twee moleculen gecombineerd en ontstaat er water (H2O) als bijproduct. Het water wordt uit het fabricageproces verwijderd omdat het de vorming van meer polymeer verhindert. De polymeerketen kan bestaan uit meer dan 20.000 monomeereenheden, aan elkaar gekoppeld door een amidegroep die een stikstofatoom bevat. Met slechts zwakke krachten, zoals waterstofbruggen, zijn de nylonmoleculen zeer flexibel tussen de polymeerketens, die de neiging hebben willekeurig in de knoop te raken. Er is geen katalysator nodig om nylon 6,6 te maken, maar zuren katalyseren de reactie; een van de monomeren is zelf een zuur. Er ontstaat een kleine reactie tussen twee moleculen adipinezuur. Om de zaken op gang te brengen, zal de ene een proton afstaan aan de carbonylzuurstof van de andere. De carbonylzuurstof wordt veel gevoeliger voor de aanval door de stikstof van de diamine wanneer deze zuurstof geprotoneerd is. Dit komt omdat de geprotoneerde zuurstof een positieve lading heeft. Zuurstof houdt er niet van positief geladen te zijn. Dus trekt het de elektronen die het deelt met de carbonyl naar zich toe. Daardoor blijft de carbonylkoolstof zonder elektronen en is bereid er een aminestikstofpaar aan over te houden.
Figuur 2: Condensatiepolymerisatie.
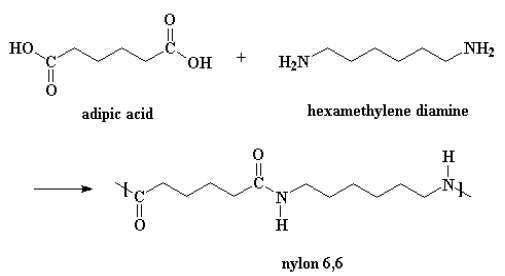
Door: (PSLC, 2019)
VERWIJDERING VANNYLON:
Na het gebruik van nylonproducten en niet langer in de vuilnisbak te willen worden gegooid, moet de mens ook een methode hebben om nylon te kunnen verwijderen. Dit levert problemen op omdat nylon een uiterst trage afnamesnelheid heeft, wat betekent dat nylonproducten zich wereldwijd ophopen op stortplaatsen. Een alternatieve techniek voor de verwijdering van nylon is daarom de verbranding ervan, maar deze techniek bevat enkele schadelijke produkten. De populairste afbraakproducten van nylon bij verhitting zijn “koolmonoxide, ammoniak, alifatische amines, ketonen, nitrillen en cyanidewaterstof”. Afhankelijk van verschillende variabelen, zoals temperatuur, blootstellingstijd en omgevingsvariabelen, kunnen sommige producten echter variëren. Zo is waterstofcyanide, een gas net boven kamertemperatuur, uiterst giftig omdat deze producten niet nuttig zijn voor de atmosfeer of de gezondheid.
VOORDELEN EN ONGEVAREN VAN NYLON:
Nylon is een veel gebruikt materiaal dat wordt gemaakt van synthetische polymeren die ook wel kunststoffen worden genoemd. Nylon is nuttig voor het maken van visnetten, touwen, parachutes en andere soorten kabels omdat het een vezel is met een hoge weerstand. Het kan ook worden gebruikt om stoffen producten te maken. Gekreukt nylon wordt gebruikt om elastische kousen te maken, en ander nylon kan zelfs als plastic worden gebruikt om machineonderdelen te maken, maar het moet met wol worden gemengd om de kracht op te voeren. Nylon heeft een lange levensduur. Het draagt goed, wat in kleding en andere stoffen een belangrijke eigenschap is. Andere producten zoals katoen of spandex kunnen ook worden gemengd. Nylon is van nature waterafstotend. Nylon heeft de neiging het naar de oppervlakte te duwen, waar het gemakkelijker verdampt, in plaats van vocht te absorberen en vast te houden zoals natuurlijke vezels. Aangezien nylon een synthetische, door de mens vervaardigde stof is in plaats van een natuurlijke stof die moet worden gekweekt of geoogst van vee, is het materiaal van nature minder duur. Hoewel het niet dezelfde uitstraling heeft als bijvoorbeeld merinowol of kasjmier, kan nylon worden geweven om een vergelijkbaar gevoel te krijgen. Bijgevolg is nylon kleding meestal minder duur dan producten die uit vergelijkbare natuurlijke bronnen worden vervaardigd.
Als u hulp nodig hebt bij het schrijven van uw essay, staat onze professionele essayschrijfdienst voor u klaar!
Meer informatie
Hoewel het gebruik van nylon veel voordelen biedt, zijn er ook enkele nadelen verbonden aan het gebruik ervan. Hoewel nylon brandwerend is, smelt het gemakkelijk. Het kan ook gemakkelijk krimpen en met vocht reageren, waardoor het te gemakkelijk kan worden uitgerekt. Nylon is hygroscopisch, dus zelfs uit lucht absorbeert het water. Nylon zwelt op en verslechtert snel als het nat is. De onderdelen mogen niet worden blootgesteld aan nylon sluitingen, wat zonlicht met zich meebrengt. Het mist UV-bestendigheid en wordt geel, ongeacht de kleur, waardoor het kwetsbaar wordt en snel achteruitgaat. Evenmin mag nylon worden blootgesteld aan uitzonderlijk hoge temperaturen. Over het algemeen zijn deze bevestigingsmiddelen slechts bestand tegen een continue gebruikstemperatuur van 121 ° F of 223 ° C, waardoor ze ongeschikt zijn voor machines of producten die tijdens het gebruik worden verwarmd, zoals die in de bouw worden gebruikt.
EVALUATIE VANNYLONIMPLICATIES EN GEBRUIKEN:
Nylon heeft vele eigenschappen die het in veel toepassingen tot een zeer nuttige vezel maken. Het is zeer krachtig en elastisch; het is ook eenvoudig te reinigen en kan over het algemeen met vergelijkbare producten worden gereinigd en er zijn over het algemeen geen speciale wasregelingen voor nodig. Als stof wordt het gebruikt in kledingsokken, zwemkleding, korte broeken, trainingsbroeken, actieve kleding, windjacks, bedspreien en draperieën. Minder vaak voorkomende toepassingen zijn onder meer flodderjacks, parachutes, gevechtsuniformen en reddingsvesten; de vezel wordt ook vaak gebruikt bij de vervaardiging van paraplu’s, bagage en netten voor bruidssluiers. Nylontextielmaterialen ontwikkelen statische elektriciteit, omdat zij niet in staat zijn voldoende watermoleculen te absorberen om de opgebouwde statische elektriciteit af te voeren. Aan de spinoplossingen worden verbindingen toegevoegd die hydroxylgroepen bevatten. De toevoeging van hydroxyl bevattende verbindingen zal een verhoogd aantal watermoleculen aantrekken.
De effecten van nylon op het milieu zijn belangrijk en moeten worden onderzocht. Bij de productie van nylon komt stikstofoxide vrij, een broeikasgas dat aanzienlijk bijdraagt tot de opwarming van de aarde. Ook is nylon niet geschikt voor natuurlijke kleurstoffen en chemische kleurstoffen met het geringste effect, wat betekent dat de methode om vezels te kleuren ook belangrijke waterverontreiniging veroorzaakt. Nu er meer nylon wordt geproduceerd in landen met een zwakkere milieubescherming, draagt nylon in belangrijke mate bij tot de waterverontreiniging en dus tot de wateronzekerheid in de ontwikkelingslanden. Nylon is niet biologisch afbreekbaar en zal eeuwig in de omgeving blijven bestaan. Nylon visnetten en synthetische textielvezels die tijdens het wassen slijten, zijn de twee grootste bronnen van micro-plasticverontreiniging in de oceaan. Dit houdt in dat nylon een belangrijk effect heeft op de aquatische omgeving. De produktie van nylon is een zeer dorstige methode; er worden grote hoeveelheden water gebruikt voor het afkoelen van de vezels, wat een oorzaak kan zijn van vervuiling en milieuverontreiniging. Een ander probleem met nylon houdt verband met de thermische verwerking; tijdens dit proces kan nylon verschillende gezondheidsproblemen veroorzaken als iemand de dampen of het stof inademt. Enkele van de problemen zijn irritatie van de slijmvliezen in neus en keel, mechanische oogirritatie en huidirritatie.
AANBEVELING/CONCLUSIE:
Nylon zal ook in de toekomst het leven van de mensen blijven beïnvloeden, maar dat kan zowel goed als slecht zijn. Vanwege zijn geweldige eigenschappen zal nylon in de toekomst nog steeds zeer nuttig zijn en er kunnen nieuwe toepassingen voor nylon komen, maar het kan nog steeds worden vervangen door andere, betere nieuwe materialen. Voor het maken van nylon zijn grote hoeveelheden water nodig om het te koelen, en daarvoor wordt een grote hoeveelheid energie gebruikt. Nylon is ook schadelijk voor het milieu, hoewel nylon zelf niet schadelijk is voor het milieu, maar de nylonmethode wel. Tijdens het fabricageproces van nylon wordt een broeikasgas gevormd, distikstofoxide genaamd, en aangezien dit materiaal nutteloos is voor de fabrieken, wordt het als afval in de atmosfeer gebracht. Lachgas heeft een levensduur van 150 jaar, zodat het in de verlaagde stratosfeer zal blijven en onze ozonlaag zal vernietigen. Een ander probleem bij de verwijdering van nylon is dat de meeste gebruikte nylonproducten op stortplaatsen terechtkomen, omdat nylon er lang over doet om te worden afgebroken en nylonproducten zich op stortplaatsen zullen ophopen. De meest efficiënte manier om nylon te vernietigen is daarom het te verbranden, maar bij deze techniek komen enkele schadelijke stoffen vrij, zoals koolmonoxide en ammoniak. Vanwege al deze problemen die gepaard gaan met het gebruik van nylon, zou het beter zijn voor het milieu om het te vervangen door ander materiaal dat niet schadelijk is.
APAReferencing
Lipscomb, D. (2019, March 14). Voordelen van Nylon. Retrieved from https://www.leaf.tv/articles/benefits-of-nylon/
Nylon 6,6 maken. (n.d.). Retrieved from https://pslc.ws/macrog/nysyn.htm
Nylon in de toekomst. (n.d.). Opgehaald van https://nylonrukunlin8dms1.weebly.com/nylon-in-the-future.html
Nylons. (n.d.). Opgehaald van https://pslc.ws/macrog/nylon.htm
Organische chemie. (n.d.). Opgehaald van https://www.merriam-webster.com/dictionary/organic chemie
Waarom is nylon nuttig? (n.d.). Ontleend aan https://nylonrukunlin8dms1.weebly.com/why-is-nylon-useful.html