三酸化硫黄の化学的性質、用途、生産
化学的性質
三酸化硫黄、S03は無水硫酸、針、ポリマーとも呼ばれ、分子種と結晶形が異なる多くの変化形で存在します。 16℃で溶ける白色の氷状のものと、33℃と62℃の高温で溶けるベストス状の2種類がある。 無色の液体または気体は刺激性の有毒ガスで、45℃(112°F)で沸騰します。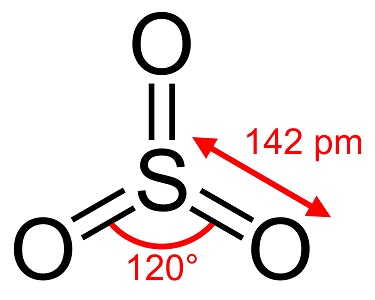
三酸化硫黄は反応性が高く、強い酸化剤であり、火災の危険性があります。 金属酸化物と反応して硫酸塩を生成し、水と反応して硫酸を生成します。 三酸化硫黄はスルホン化反応に使用される。
物理的性質
常温、常圧では無色の液体で、空気中で発煙する。
三酸化硫黄は特に微量の水または硫酸の存在下で重合する傾向がある。 しかし、その重合速度は凝固点に近づくにつれて大きく減少する。 固体の三酸化硫黄はα相、β相、γ相の3つの多形態で存在する。
α相は高分子架橋構造を持つ氷状の針状物質からなる。 β相は高分子分子からなる白色でアスベスト様の光沢のある針状で、32.5℃で融解し、25℃で蒸気圧344torrの準安定同素体です。 固体の場合は16.8℃で融解するコロイド状の氷のような塊である。 液体では1.9224g/mLの密度を持ち、44.8℃で沸騰します。 25℃での蒸気圧は433torrである。 ガンマ相は環状三量体と単量体の分子からなる。 固体の三酸化硫黄が溶けるとγ相になり、固化するとα相になる。
SO3の臨界温度は217.8℃、臨界圧力80.97 atm、臨界密度0.63 g/cm3、18℃の液体SO3の誘電率は3.11
三酸化硫黄が水に溶けて硫酸となり大きな発熱を伴うが、硫酸は水中に溶けるので、硫酸塩と同じように発熱する。
用途
三酸化硫黄は硫酸およびスルホン化用オレオンの製造、特に染料および染料の製造、無水硝酸および爆薬の製造の中間体として使用される。 固体三酸化硫黄は、Sulphan、Triosulなどの名称で販売され、主に有機酸のスルホン化に使用されます。 四フッ化硫黄はフッ素化剤である。 六フッ化硫黄は高圧電気設備の気体絶縁体として使用されます。 フッ化スルフィリルは殺虫剤および燻蒸剤として使用されます。
有機化合物のスルホン化、特に非イオン性洗剤、太陽エネルギーコレクター。 通常、使用する工場で生成される。
製造方法
三酸化硫黄は硫酸を製造する際の中間体として接触法(硫酸の項参照)により製造される。
三酸化硫黄は実験室で発煙硫酸を加熱し、その蒸気を凝縮させ、冷却レシーバーに回収することにより調製される。 蒸気が微量の水分の存在下で27℃以下に凝縮されると、SO3の3つの多形相がすべて生成される。 これらは分留により分離することができる。 27℃以上の蒸気が凝縮すると、液状の三酸化ガンマ硫黄が生成される。
一般的な説明
三酸化硫黄は無色から白色の結晶性固体で、空気中で発煙します。 重合防止剤と一緒に出荷されることが多いです。 三酸化硫黄は水と激しく反応し、熱を放出して硫酸を生成します。 三酸化硫黄は金属や組織に対して腐食性がある。 三酸化硫黄は、目や皮膚に火傷を負わせる。 飲み下すと、口、食道、胃に重度の火傷を負わせる。 蒸気は吸入すると非常に有毒である。 三酸化硫黄は、木材、綿、繊維板などの有機物と接触すると火災の危険性がある。
空気 & 水反応
爆発的な力で水と結合し、その酸性のために硫酸を形成する 三酸化硫黄はほとんどの有機物を炭化する。 空気中に放置すると、三酸化硫黄は急速に吸湿し、濃厚な白煙が発生する。
Reactivity Profile
三酸化硫黄と二弗化酸素の反応は非常に激しく、溶媒がない状態で反応を行うと爆発を起こす。 三酸化硫黄とテトラフルオロエチレンとの過剰の反応は爆発的な分解を起こし、フッ化カルボニルと二酸化硫黄になります。 無水過塩素酸と三酸化硫黄の反応は激しく、かなりの熱の発生を伴う(Pascal 16:300 1931-34)。 液状の三酸化硫黄は塩化ニトリルと75℃でも激しく反応し、三酸化硫黄と酸化鉛の反応では白色発光を起こす。 ヨウ素、ピリジン、三酸化硫黄、ホルムアミドの組み合わせでは、数ヵ月後に加圧しすぎてガスが発生した。 これは、外部からの水分による硫酸の生成やホルムアミドのシアン化水素への脱水が遅いためである。
危険
酸化剤、無機物との接触で火災の危険性、α形が溶けるときに蒸気圧の爆発的な増加が発生する。 無水物は水と結合して硫酸を生成し、熱を発生させる。 毒性が強く、組織を強く刺激する。
Health Hazard
三酸化硫黄は毒性が強い。 粘膜を刺激し、腐食性がある。 吸入または飲み込むと毒性。 接触すると皮膚や目に重度の火傷を負わせる。
火災の危険性
有機物との接触により火災の危険がある。 α形が溶けると爆発的な蒸気圧の上昇を起こす。 水と化合して爆発的な暴力を持ち、硫酸を生成する。 他の可燃物(木材、紙、油など)を発火させることがある。 タンク、ホッパー車内に引火性有毒ガスが蓄積するおそれがある。 下水道に流出すると火災や爆発の危険がある。 水と接触すると硫酸を生成する。 水や有機物を避ける。 空気に触れると、三酸化硫黄は水分を吸収し、濃い白色のヒュームを発生させる。
Safety Profile
吸入すると中毒を起こす。 吸入による人体への影響:咳、その他の肺および嗅覚の変化。 皮膚、眼、粘膜に腐食性の刺激物。 O2F2、PbO、NClO2、HClO4、P、テトラフルオロエチレン、アセトニトリル、硫酸、ジメチルスルホキシド、ジオキサン、水、ジフェニル水銀、ホルムアミド、ヨウ素、ピリジン、金属酸化物とは激しく反応する。 蒸気と反応して腐食性の有毒な硫酸のヒュームを形成する。 加熱して分解すると有毒なSO,の蒸気を発生する。 SULFURIC ACIDの項も参照。
潜在的暴露
三酸化硫黄は、洗剤、潤滑油添加剤、その他の有機化合物の硫酸化剤およびスルホン化剤として、太陽エネルギー回収装置で使用されています。 また、硫酸製造の中間体や火薬の製造にも使用されます。
storage
三酸化硫黄の蒸気圧は温度の上昇とともに急速に上昇し、α形が融解すると圧力上昇は爆発的であるため、輸送および貯蔵容器には10~15気圧の圧力に耐えるものが要求される。 三酸化硫黄は水と激しく高熱で反応し、ヒドロ硫酸を生成する。 湿った空気に触れると発煙し、硫酸のミストを形成し、やがて利用可能な空間すべてを満たす。また、金属を腐食する。 強力な酸化剤であり、液相では有機物を炭化する。
Shipping
UN1829 三酸化硫黄、安定化、ハザードクラス: 8; ラベル 8-腐食性物質、6.1-毒物吸入の危険、吸入危険ゾーンB
Incompatibility
可燃性、腐食性がある。 強酸化剤。 水、蒸気、水分と激しく反応し、腐食性のヒドロサルファイド酸を発生する。 強塩基、強酸、化学的に活性な金属、還元剤、微細な金属、シアン化物、硝酸塩、ピクレート、フルミネート、塩素酸塩、硫化物、炭化物、リン、二フッ化二酸素、酸化バリウム、酸化鉛、ジフェニル水銀、アルコール、塩化ニトリル、アセトニトリル、ジオキサン、テトラフルオロエチレンとの接触で激しい反応に見舞われる。
廃棄物処理
詰め替え可能な圧縮ガスボンベは、供給者に返却すること。 詰め替えられないボンベは、地方、州、および連邦政府の規則に従って処分する必要があります。 残ったガスは、密閉されていない場所、または排気フードでゆっくりと大気中に放出させる。 詰め替えタイプのシリンダーは、バルブキャップとコンセントプラグが固定され、バルブ保護キャップが設置された状態で、元の供給者に返却する必要があります。