- Triossido di zolfo Proprietà chimiche, usi, produzione
- Proprietà chimiche
- Proprietà fisiche
- Usi
- Metodi di produzione
- Descrizione generale
- Aria &Reazioni con l’acqua
- Profilo di reattività
- Pericolo
- Pericolo per la salute
- Rischio d’incendio
- Profilo di sicurezza
- Esposizione potenziale
- Stoccaggio
- Spedizione
- Incompatibilità
- Smaltimento dei rifiuti
Triossido di zolfo Proprietà chimiche, usi, produzione
Proprietà chimiche
Il triossido di zolfo, S03, noto anche come anidride solforica, aghi o polimero, esiste in una serie di modificazioni che differiscono per specie molecolare e forma cristallina. Ha una modifica bianca, simile al ghiaccio, che si scioglie a 16°C (61°F) e altre due forme simili al bestos che si sciolgono alle temperature più alte di 33 e 62°C (90 e 144°F). La forma incolore liquida o gassosa ha fumi irritanti e tossici e bolle a 45 °C (112 °F).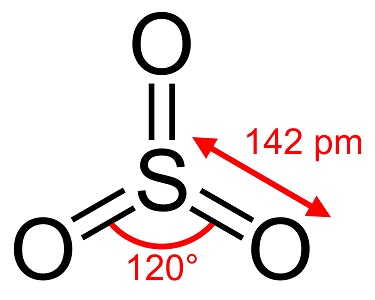
Il triossido di zolfo è una sostanza altamente reattiva, un forte agente ossidante e un pericolo di incendio. Reagisce con gli ossidi metallici per formare solfati e con l’acqua per formare acido solforico. Il triossido di zolfo è usato per la solfonazione.
Proprietà fisiche
Liquido incolore a temperatura ambiente e pressione atmosferica; fumi in aria.
Il triossido di zolfo tende a polimerizzare, particolarmente in presenza di tracce di acqua o acido solforico. Il tasso della sua polimerizzazione, tuttavia, diminuisce notevolmente quando il suo punto di congelamento si avvicina. Il triossido di zolfo solido (polimerico) esiste in tre fasi polimorfiche: modifiche alfa, beta e gamma.
La fase alfa è costituita da aghi simili al ghiaccio con struttura polimerica reticolata. Fonde a 62,3°C e ha una pressione di vapore di 73 torr a 25°C.
La fase beta è un allotropo metastabile con aghi bianchi, simili all’amianto, lucenti, composti da molecole polimeriche, che fonde a 32,5°C, e con una pressione di vapore di 344 torr a 25°C.
La modifica gamma a temperature ordinarie può esistere in forma solida o liquida. In forma solida è una massa colloidale simile al ghiaccio che fonde a 16,8°C. Nella forma liquida ha una densità di 1,9224 g/mL, ebollizione a 44,8°C. Ha una pressione di vapore di 433 torr a 25°C. La fase gamma consiste in molecole di trimer e monomeri ciclici. Quando il triossido di zolfo solido si fonde, si converte nella sua fase gamma che alla solidificazione passa alla modifica alfa.
La temperatura critica di SO3 è 217,8°C; pressione critica 80,97 atm; densità critica 0,63 g/cm3; la costante dielettrica di SO3 liquido a 18°C è 3,11.
Il triossido di zolfo si dissolve in acqua formando acido solforico e generando grande calore.
Usi
Il triossido di zolfo è usato come intermedio nella fabbricazione dell’acido solforico e dell’oleum per la solfonazione, in particolare, di coloranti e materie coloranti, e per la produzione di acido nitrico anidro e di esplosivi. Il triossido di zolfo solido è commercializzato con nomi come Sulphan e Triosul, ed è usato principalmente per la solfonazione degli acidi organici. Il tetrafluoruro di zolfo è un agente di fluorizzazione. L’esafluoruro di zolfo serve come isolante gassoso negli impianti elettrici ad alta tensione. Il fluoruro di solfirile è usato come insetticida e fumigante.
Sulfonazione di composti organici, specialmente detergenti non ionici, collettori di energia solare. Di solito viene generato nell’impianto in cui deve essere utilizzato.
Metodi di produzione
Il triossido di zolfo è prodotto come intermedio nella fabbricazione dell’acido solforico tramite il processo di contatto (vedi Acido solforico). Il processo comporta l’ossidazione catalitica dell’anidride solforosa a triossido.
Il triossido di zolfo è preparato in laboratorio riscaldando l’acido solforico fumante, condensando i suoi vapori e raccogliendoli in un ricevitore freddo. Quando i vapori vengono condensati sotto i 27°C in presenza di tracce di umidità, vengono prodotte tutte e tre le fasi polimorfe di SO3. Esse possono essere separate per distillazione frazionata. La condensazione dei vapori sopra i 27°C forma la varietà liquida del triossido di zolfo gamma.
Descrizione generale
Il triossido di zolfo è un solido cristallino da incolore a bianco che fuma in aria. Spesso viene spedito con un inibitore per prevenire la polimerizzazione. Il triossido di zolfo reagisce violentemente con l’acqua per formare acido solforico con il rilascio di calore. Il triossido di zolfo è corrosivo per i metalli e i tessuti. Il triossido di zolfo causa ustioni agli occhi e alla pelle. L’ingestione causa gravi ustioni alla bocca, all’esofago e allo stomaco. Il vapore è molto tossico per inalazione. Il triossido di zolfo è un rischio di incendio se a contatto con materiali organici come legno, cotone, cartone di fibra, ecc.
Aria &Reazioni con l’acqua
Si combina con l’acqua con forza esplosiva, formando acido solforico a causa della sua acidità Il triossido di zolfo carbonizza la maggior parte delle sostanze organiche. All’esposizione all’aria il triossido di zolfo assorbe rapidamente l’umidità, emettendo densi fumi bianchi.
Profilo di reattività
La reazione del triossido di zolfo e del difluoruro di ossigeno è molto vigorosa e si verificano esplosioni se la reazione è effettuata in assenza di un solvente. La reazione del triossido di zolfo in eccesso con il tetrafluoroetilene causa una decomposizione esplosiva a fluoruro di carbonile e biossido di zolfo. La reazione dell’acido perclorico anidro con il triossido di zolfo è violenta e accompagnata dall’evoluzione di un calore considerevole (Pascal 16:300 1931-34). Il triossido di zolfo liquido reagisce violentemente con il cloruro di nitrile, anche a 75° C. La reazione del triossido di zolfo con l’ossido di piombo causa una luminescenza bianca. La combinazione di iodio, piridina, triossido di zolfo e formammide ha sviluppato un gas in sovrapressione dopo diversi mesi. Ciò è dovuto alla lenta formazione di acido solforico, dall’acqua esterna o dalla disidratazione della formammide in cianuro di idrogeno.
Pericolo
Agente ossidante, rischio di incendio a contatto con materiali organici, un aumento esplosivo della pressione del vapore si verifica quando la forma α si fonde. L’anidride si combina con l’acqua, formando acido solforico e sviluppando calore. Altamente tossico, forte irritante per i tessuti.
Pericolo per la salute
Il triossido di zolfo è altamente tossico. È un irritante e corrosivo per le membrane mucose. Velenoso se inalato o ingerito. Il contatto causa gravi ustioni alla pelle e agli occhi.
Rischio d’incendio
Rischio d’incendio a contatto con materiali organici. Un aumento esplosivo della pressione del vapore si verifica quando la forma alfa si fonde. Si combina con l’acqua con violenza esplosiva, formando acido solforico. Può infiammare altri materiali combustibili (legno, carta, olio, ecc.). I gas velenosi infiammabili possono accumularsi nei serbatoi e nei vagoni tramoggia. Il deflusso nelle fognature può creare pericolo di incendio o esplosione. Forma acido solforico a contatto con l’acqua. Evitare acqua e materiali organici. In caso di esposizione all’aria, il triossido di zolfo assorbe l’umidità ed emette fumi bianchi densi.
Profilo di sicurezza
Veleno per inalazione. Effetti sistemici umani per inalazione: tosse e altri cambiamenti polmonari e olfattivi. Irritante corrosivo per la pelle, gli occhi e le membrane mucose. Reazione violenta con O2F2, PbO, NClO2, HClO4, P, tetrafluoretilene, acetonitrile, acido solforico, dimetilsolfossido, diossano, acqua, difenilmercurio, formamide, iodio, piridina, ossidi metallici. Reagisce con il vapore per formare fumi corrosivi e tossici di acido solforico. Se riscaldato fino alla decomposizione emette fumi tossici di SO,. Vedere anche ACIDO SOLFORICO.
Esposizione potenziale
Il triossido di zolfo è usato come agente solfatante e solfonante per detergenti, additivi per oli lubrificanti e altri composti organici; nei collettori di energia solare. È anche usato come intermedio nella produzione di acido solforico e nella fabbricazione di esplosivi.
Stoccaggio
La pressione del vapore del triossido di zolfo aumenta rapidamente con l’aumento della temperatura e, quando la forma α si fonde, l’aumento di pressione è esplosivo; di conseguenza i contenitori per il trasporto e lo stoccaggio devono sopportare pressioni da 10 a 15 atm. Il triossido di zolfo reagisce vigorosamente e altamente esotermico con l’acqua per produrre acido idrosolforico. Quando è esposto all’aria umida, esala e forma una nebbia di acido solforico che alla fine riempie tutto lo spazio disponibile; inoltre corrode i metalli. È un potente agente ossidante e, in fase liquida, carbonizza i materiali organici.
Spedizione
UN1829 Triossido di zolfo, stabilizzato, Classe di pericolo: 8; Etichette: 8-Materiale corrosivo, 6.1-Pericolo di inalazione, Pericolo di inalazione Zona B.
Incompatibilità
Combustibile e corrosivo. Un forte ossidante. Reagisce violentemente con acqua, vapore o umidità, rilasciando acido idrosolforico corrosivo. Reazioni violente si verificano a contatto con basi forti, acidi forti, metalli chimicamente attivi, agenti riducenti, metalli finemente divisi, cianuri, nitrati, picrati, fulminati, clorati, solfuri, carburi, fosforo, difluoruro di diossido, ossido di bario, ossido di piombo, mercurio difenile, alcoli, cloruro di nitrile, acetonitrile, diossano, tetrafluoroetilene.
Smaltimento dei rifiuti
Restituire le bombole di gas compresso ricaricabili al fornitore. Le bombole non ricaricabili devono essere smaltite in conformità alle normative locali, statali e federali. Lasciare che il gas rimanente sfoghi lentamente nell’atmosfera in un’area non confinata o in una cappa di aspirazione. Le bombole ricaricabili devono essere restituite al fornitore originale con tutti i tappi delle valvole e i tappi di uscita fissati e i cappucci di protezione delle valvole al loro posto.