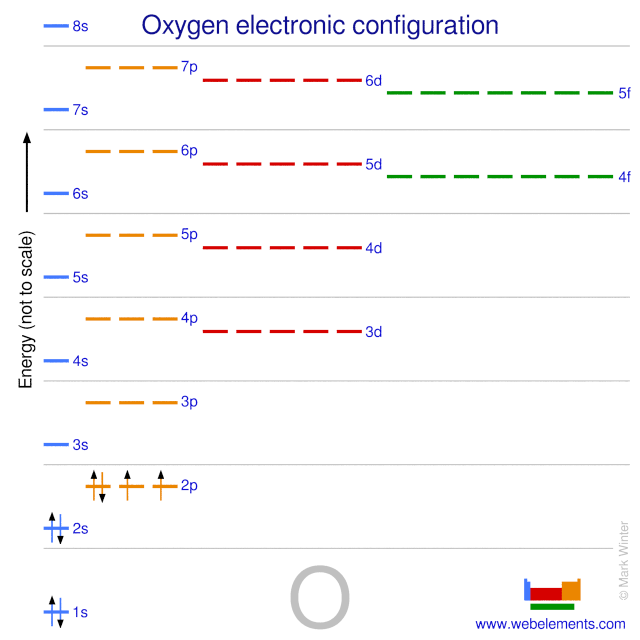
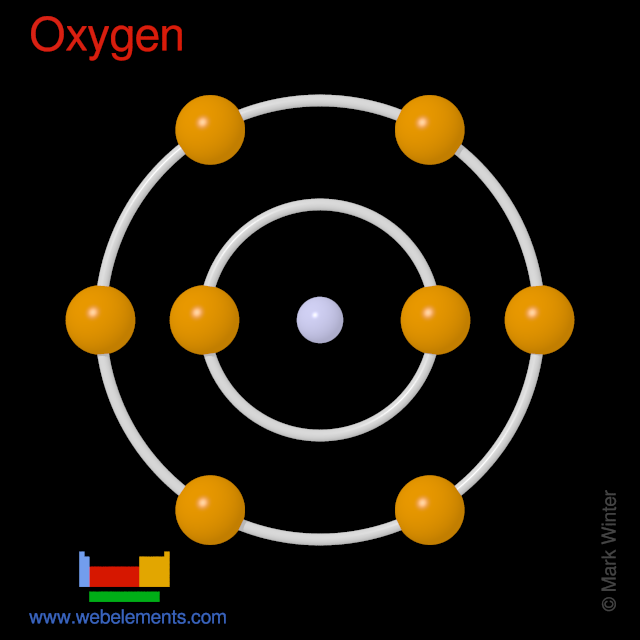
Gli atomi di ossigeno hanno 8 elettroni e la struttura a guscio è 2.6.
La configurazione elettronica dello stato di terra dell’ossigeno neutro gassoso è .2s2.2p4 e il termine simbolo è 3P2.
Spettro atomico
Una rappresentazione dello spettro atomico dell’ossigeno.
Energie di ionizzazione e affinità elettronica
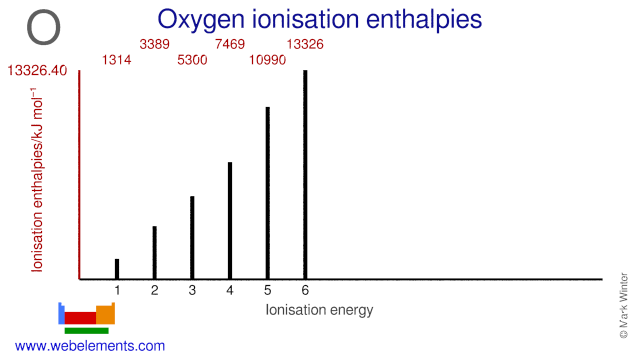
L’affinità elettronica dell’ossigeno è 141 kJ mol-1. Le energie di ionizzazione dell’ossigeno sono date qui sotto.
| Numero di energia di ionizzazione | Enthalpy / kJ mol-1 |
|---|---|
| 1st | 1313.94 |
| 2° | 3388.67 |
| 3° | 5300.47 |
| 4° | 7469.27 |
| 5° | 10989.6 |
| 6° | 13326.4 |
| 7° | 71334.2 |
| 8° | 84078.3 |
Cariche nucleari effettive
Le seguenti sono cariche nucleari effettive “Clementi-Raimondi”, Zeff. Seguire i collegamenti ipertestuali per ulteriori dettagli e per i grafici in vari formati.
| 1s | 7.6579 | ||||||
|---|---|---|---|---|---|---|---|
| 2s | 4.49 | 2p | 4.45 | ||||
| 3s | (nessun dato) | 3p | (nessun dato) | 3d | (nessun dato) | ||
| 4s | (nessun dato) | 4p | (nessun dato) | 4d | (nessun dato) | 4f | (nessun dato) |
| 5s | (nessun dato) | 5p | (nessun dato) | 5d | (nessun dato) | ||
| 6s | (nessun dato) | 6p | (nessun dato) | ||||
| 7s | |||||||
Queste cariche nucleari efficaci, Zeff, sono adattate dai seguenti riferimenti:
- E. Clementi e D.L.Raimondi, J. Chem. Phys. 1963, 38, 2686.
- E. Clementi, D.L.Raimondi, e W.P. Reinhardt, J. Chem. Phys. 1967, 47, 1300.
Energie di legame degli elettroni
| Etichetta | Orbitale | eV |
|---|---|---|
| K | 1s | 543.1 |
| L I | 2s | 41.6 |
Note
Sono grato a Gwyn Williams (Jefferson Laboratory, Virginia, USA) che ha fornito i dati sull’energia di legame degli elettroni. I dati sono adattati dai riferimenti 1-3. Sono tabulati altrove sul WWW (riferimento 4) e in forma cartacea (riferimento 5).
- J. A. Bearden e A. F. Burr, “Reevaluation of X-Ray Atomic Energy Levels”, Rev. Mod. Phys., 1967, 39, 125.
- M. Cardona e L. Ley, Eds., Photoemission in Solids I: General Principles (Springer-Verlag, Berlin) con ulteriori correzioni, 1978.
- Gwyn Williams WWW tabella dei valori
- D.R. Lide, (Ed.) in Chemical Rubber Company handbook of chemistry and physics, CRC Press, Boca Raton, Florida, USA, 81a edizione, 2000.
- J. C. Fuggle e N. Mårtensson, “Core-Level Binding Energies in Metals,” J. Electron Spectrosc. Relat. Phenom., 1980, 21, 275.