Edellisessä jaksossa on kerrottu, miten eri alkuaineet voivat joko olla olemassa yksinään tai yhdistyä toisten alkuaineiden kanssa yhdisteiksi. Tämä jakso perustuu näihin ajatuksiin tarkastelemalla kemiallisia reaktioita yksityiskohtaisemmin. Se osoittaa myös, miten kemiallisia lyhenteitä voidaan laajentaa kuvaamaan kemiallisia reaktioita.
Katsotaan ensin joitakin aiemmin kuvattuja molekyylejä: vesi, metaani, hiilidioksidi ja ammoniakki.
Kysymys 26
Minkälaiset ovat kunkin näistä neljästä molekyylistä muodostamat kaavat?
Vastaus
Kaavat ovat vastaavasti H2O, CH4, CO2 ja NH3.
Vaikka sinun ei tarvitse muistaa tällä kurssilla esiteltyjen yhdisteiden kemiallisia kaavoja, on luultavasti hyödyllistä painaa mieleen muutamia, kuten edellä mainittujen neljän molekyylin sekä vety- (H2), typpi- (N2) ja happimolekyylien (O2) kaavat. Tämä auttaa sinua näiden kemiallisten kaavojen lukemisessa ja kirjoittamisessa ilman, että joudut jatkuvasti palaamaan aiempiin osioihin.
Katselet nyt reaktioita, joissa ovat mukana alkuaineet vety, hiili ja happi sekä yhdisteet metaani, vesi ja hiilidioksidi.
Vety reagoi hapen kanssa, kun se sytytetään tuleen (se on melko räjähdysherkkää), jolloin muodostuu vettä. Jotta tällainen reaktio voidaan kirjoittaa kemiallisen yhtälön avulla, laitetaan vasemmalle puolelle aineet, jotka käyvät läpi reaktion, ja oikealle puolelle aineet, jotka reaktiossa syntyvät. Vasemmalla olevat reagoivat aineet yhdistetään oikealla oleviin tuotteisiin nuolella.
Yhtälö voidaan kirjoittaa sanayhtälönä ”vety ja happi muodostavat vettä”, tai käyttämällä hieman kemiallista pikakirjoitusta se voidaan kirjoittaa seuraavasti:

jossa nuoli tarkoittaa ”menee”.
Kokeile nyt kemiallista pikakirjoitusta yhtälön kirjoittamiseen. Korvaamalla symbolit sanayhtälöllä saadaan:

Yhtälössä nuolen vasemmalla puolella olevat reagoivat aineet muuttuvat oikealla puolella olevaksi tuotteeksi. Tässä yhtälössä on kuitenkin jotain vikaa. Voit nähdä, mikä on pielessä, kun katsot kuvaa 21, jossa reaktantit ja tuotteet on esitetty kaaviona.
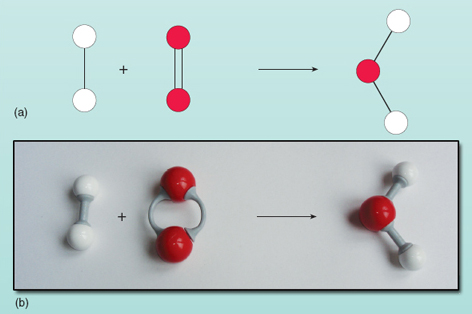
Laskemalla atomien lukumäärät yhtälön kummallakin puolella nähdään, että vasemmalla puolella on kaksi happiatomia ja oikealla puolella yksi. Yhtälön molemmilla puolilla olevien happiatomien lukumäärän on oltava yhtä suuri – ne eivät voi maagisesti ilmestyä ja kadota reaktion aikana. Yhtälön oikealla puolella olevan vesimolekyylin koostumusta ei voi muuttaa, koska vesimolekyyli on olemassa kahden vetyatomin ja yhden happiatomin muodostamana ryhmänä, jotka ovat kaikki sitoutuneet toisiinsa. Jokainen happimolekyyli toimittaa kaksi happiatomia, joten se muodostaa aina kaksi vesimolekyyliä, jos sen kanssa reagoi kaksi vetymolekyyliä (kukin on kahden atomin yksikkö). Kahden vesimolekyylin muodostamiseen tarvitaan siis kaksi vety- ja yksi happimolekyyli. Reaktio ilmaistaan tarkasti seuraavasti:

Yhtälön molemmilla puolilla on nyt sama määrä kumpaakin atomityyppiä: kemiallinen yhtälö on tasapainossa, joten voimme nyt korvata nuolen yhtäsuuruusmerkillä.
Viimeinen parannus, jolla vältetään yhtälön vasemmanpuoleisten vety- ja oikeanpuoleisten vesimolekyylien toistuminen, on se, että ne merkitään yhtälössä muodossa: 2H2 H2 + H2 sijaan. Näin tasapainotettu kemiallinen yhtälö muuttuu:

Tämä on esitetty kaavamaisesti kuvassa 22.

Kemialliset yhtälöt osoittavat hyvin tiiviisti paitsi sen, mitkä atomit ja molekyylit reagoivat keskenään muodostaen tuotteita, myös sen, kuinka monta kutakin atomi- ja molekyylilajia on mukana. On tärkeää muistaa, että molekyylin edessä oleva numero tarkoittaa kyseisen molekyylin lukumäärää. Esimerkiksi 3H2O tarkoittaa kolmea vesimolekyyliä, jolloin vety- ja happiatomeja on yhteensä kuusi ja happiatomeja kolme.
Kemiallisen yhtälön on oltava tasapainossa; kummankin alkuainetyypin atomien lukumäärän yhtälön molemmilla puolilla on oltava yhtä suuri.
Tiedät nyt, miten kemiallista yhtälöä ”luetaan” tai tulkitaan eli miten se kuvaa kemian prosessia. Kemistit ovat kuitenkin myös erittäin taitavia kirjoittamaan kemiallisia yhtälöitä eräänlaisena pikakirjoituksena kuvaamaan erilaisia kemiallisia prosesseja tai reaktioita. Kemiallisten yhtälöiden kirjoittaminen on kuin minkä tahansa vieraan kielen kirjoittaminen – se vaatii harjoittelua, jotta siitä tulisi sujuvaa. Kaikkien aloittelevien tiedemiesten on kuitenkin aloitettava jostain, ja alla olevassa osiossa näytetään, miten se onnistuu hyvin tutun kemiallisen reaktion avulla. Jos haluat tarkistaa, tarvitseeko sinun opiskella tätä jaksoa, kokeile ensin kysymystä 20.