Pojmenování alkoholů
- Najděte nejdelší řetězec obsahující hydroxyskupinu (OH). Pokud existuje řetězec s více uhlíky než ten, který obsahuje skupinu OH, bude pojmenován jako podřazený.
- Uveďte OH na nejnižším možném čísle řetězce. S výjimkou karbonylových skupin, jako jsou ketony a aldehydy, mají při pojmenování přednost alkoholové nebo hydroxylové skupiny.
- Při pojmenování cyklické struktury se předpokládá, že -OH je na prvním uhlíku, pokud není přítomna karbonylová skupina, v takovém případě dostane na prvním uhlíku přednost později uvedená skupina.
- Pokud je na cyklické struktuře více skupin -OH, očíslujte uhlíky, na kterých se nacházejí skupiny -OH.
- Z mateřského řetězce alkanů odstraňte koncové e a přidejte -ol. Pokud je přítomno více alkoholů, použijte di, tri, et.c před ol, za mateřským názvem. např. 2,3-hexandiol. Pokud je přítomna karbonylová skupina, pojmenovává se skupina -OH s předponou „hydroxy“, přičemž karbonylová skupina se připojí k názvu mateřského řetězce tak, že končí na -al nebo -one.
Příklady
Etan: CH3CH3 —–>Etanol: 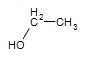 (alkohol obsažený v pivu, víně a dalších konzumovaných lihovinách)
(alkohol obsažený v pivu, víně a dalších konzumovaných lihovinách)
Sekundární alkohol: 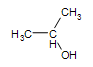 2-propanol
2-propanol
Další funkční skupiny na alkoholu: 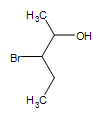 3-bromo-2-pentanol
3-bromo-2-pentanol
Cyklický alkohol (dvě skupiny -OH): 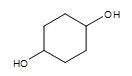 cyklohexan-1,4-diol
cyklohexan-1,4-diol
Jiná funkční skupina na cyklické struktuře:
Složitý alkohol: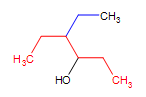 4-ethyl-3hexanol (mateřský řetězec je červeně a substituent modře)
4-ethyl-3hexanol (mateřský řetězec je červeně a substituent modře)
V nomenklaturním systému IUPAC se funkční skupiny obvykle označují jedním ze dvou způsobů. Přítomnost funkce může být označena charakteristickou příponou a číslem umístění. To je běžné pro dvojnou a trojnou vazbu uhlík-uhlík, které mají příslušné přípony -en a -yne. Naproti tomu halogeny příponu nemají a pojmenovávají se například jako substituenty: (CH3)2C=CHCHClCH3 je 4-chlor-2-methyl-2-penten.
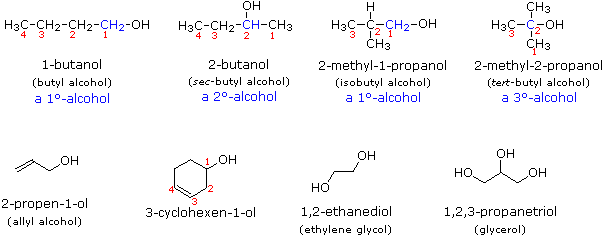
Alkoholy se obvykle pojmenovávají prvním postupem a označují se příponou -ol, jako např. ethanol, CH3CH2OH (všimněte si, že u dvouuhlíkatého řetězce není lokalizační číslo nutné). U delších řetězců určuje číslování řetězce umístění hydroxylové skupiny. Například: (CH3)2C=CHCH(OH)CH3 je 4-methyl-3-penten-2-ol. Další příklady názvosloví IUPAC jsou uvedeny níže spolu s běžnými názvy, které se často používají pro některé jednodušší sloučeniny. Pro monofunkční alkoholy se tento běžný systém skládá z pojmenování alkylové skupiny následované slovem alkohol. Alkoholy lze také klasifikovat jako primární, 1º, sekundární, 2º, a terciární, 3º, stejným způsobem jako alkylhalogenidy. Tato terminologie se vztahuje k alkylové substituci atomu uhlíku nesoucího hydroxylovou skupinu (na obrázku je zbarven modře).
Mnoho funkčních skupin má charakteristické příponové označení a v názvu může být použita pouze jedna taková přípona (jiná než „-en“ a „-yne“). Pokud je hydroxylová funkční skupina přítomna společně s funkcí s vyšší prioritou nomenklatury, musí být uvedena a lokalizována pomocí předpony hydroxy a příslušného čísla. Například kyselina mléčná má podle IUPAC název kyselina 2-hydroxypropanová.
Název ethery
Ethery jsou sloučeniny, které mají dvě alkylové nebo arylové skupiny vázané na atom kyslíku, jako ve vzorci R1-O-R2. Éterová funkční skupina nemá charakteristickou příponu názvosloví IUPAC, proto je nutné ji označit jako substituent. Za tímto účelem jsou běžným alkoxy substituentům přiřazeny názvy odvozené od jejich alkylové složky (níže):
| Alkylová skupina | Název | Alkoxy skupina | Název | ||
|---|---|---|---|---|---|
| CH3- | Methyl | CH3O- | Methoxy | ||
| CH3CH2- | Ethyl | CH3CH2O- | Etoxy | ||
| (CH3)2CH- | Izopropyl | (CH3)2CHO- | Izopropoxy | ||
| (CH3)3C- | terc-Butyl | (CH3)3CO- | tert-Butoxy | ||
| C6H5- | Fenyl | C6H5O- | Fenoxy |
Menší, kratší alkylová skupina se stává alkoxy substituentem. Větší, delší strana alkylové skupiny se stává názvem alkanové báze. Každá alkylová skupina na každé straně kyslíku je číslována samostatně. Přednost při číslování má uhlík, který je nejblíže oxgenu. Alkoxidová strana (kratší strana) má koncovku „-oxy“ s příslušnou alkylovou skupinou. Například CH3CH2CH2CH2CH2-O-CH2CH2CH3 je 1-propoxypentan. Pokud existuje cis nebo trans stereochemie, stále platí stejné pravidlo.
Příklad 9.3.1
Příklady jsou: CH3CH2OCH2CH3, diethylether (někdy označovaný jako ether), a CH3OCH2CH2OCH3, ethylenglykol-dimethylether (glym).
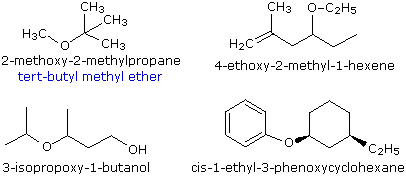
Obvyklé názvy
Jednotlivé ethery mají běžné názvy, v nichž jsou alkylové skupiny vázané na kyslík pojmenovány v abecedním pořadí a následuje slovo „ether“. Příklad vlevo nahoře ukazuje běžný název modře pod názvem IUPAC. Mnoho jednoduchých etherů je symetrických v tom smyslu, že oba alkylové substituenty jsou stejné. Ty se nazývají „dialkylethery“.
Heterocykly
V cyklických etherech (heterocyklech) je jeden nebo více uhlíků nahrazeno kyslíkem. Často se hovoří o heteroatomech, kdy je uhlík nahrazen kyslíkem nebo jiným atomem než uhlíkem nebo vodíkem. V tomto případě se kmen nazývá oxacykloalkan, kde předpona „oxa-“ je indikátorem nahrazení uhlíku kyslíkem v kruhu. Tyto sloučeniny se číslují od kyslíku a pokračují kolem kruhu. Například,

Pokud je substituentem alkohol, má alkohol vyšší prioritu. Pokud je však substituentem halogenid, má vyšší prioritu éter. Pokud je v substituentu jak alkoholová skupina, tak halogenid, má vyšší prioritu alkohol. Číslování začíná koncem, který je nejblíže substituentu s vyšší prioritou. Existují étery, které obsahují více éterových skupin a nazývají se cyklické polyethery nebo korunové étery. Ty jsou také pojmenovány podle systému IUPAC.
hyl sulfid. Sulfidy jsou chemicky reaktivnější než ethery, což odráží větší nukleofilitu síry oproti kyslíku.
Problémy
Nejmenujte následující ethery:
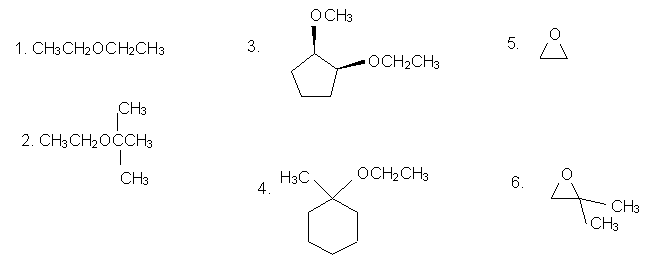
(Odpovědi na výše uvedené problémy: 1. diethylether; 2. 2-ethoxy-2-methyl-1-propan; 3. cis-1-ethoxy-2-methoxycyklopentan; 4. 1-ethoxy-1-methylcyklohexan; 5. oxycyklopropan; 6. 2,2-dimethyloxacyklopropan)
Obvyklé názvy některých etherů
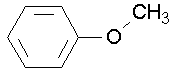
anizol (zkuste pojmenovat anizol podle dalších dvou konvencí. J )
oxiran
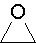
1,2-epoxyethan, ethylenoxid, dimethylenoxid, oxacyklopropan,
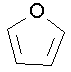
furan (tato sloučenina je aromatická)
tetrahydrofuran

oxacyklopentan, 1,4-epoxybutan, tetrametylenoxid,
dioxan

1,4-dioxacyklohexan
Přispěvatelé
- Abhiram Kondajji (UCD)
-
William Reusch, emeritní profesor (Michigan State U.), Virtuální učebnice organické chemie