Cíle výuky
- Ukázat a pojmenovat jednoduché (přímočaré) alkany podle vzorců a napsat vzorce pro přímočaré alkany podle jejich názvů.
Studium organické chemie začínáme uhlovodíky, nejjednoduššími organickými sloučeninami, které jsou tvořeny pouze atomy uhlíku a vodíku. Jak jsme si již poznamenali, existuje několik různých druhů uhlovodíků. Rozlišují se podle typů vazeb mezi atomy uhlíku a vlastností, které z těchto vazeb vyplývají. Uhlovodíky, které mají pouze jednoduché vazby mezi uhlíky (C-C) a existují jako souvislý řetězec atomů uhlíku vázaných také na atomy vodíku, se nazývají alkany (nebo nasycené uhlovodíky). Nasycený v tomto případě znamená, že každý atom uhlíku je vázán na čtyři další atomy (vodíku nebo uhlíku) – což je nejvíce možné; v molekulách nejsou žádné dvojné nebo trojné vazby.
Slovo nasycený má pro uhlovodíky stejný význam jako pro potravinářské tuky a oleje: molekula nemá žádné dvojné vazby mezi uhlíky (C=C).
Tři nejjednodušší alkany-metan (CH4), etan (C2H6) a propan (C3H8) jsme již dříve představili a jsou opět zobrazeny na obrázku \(\PageIndex{1}\).
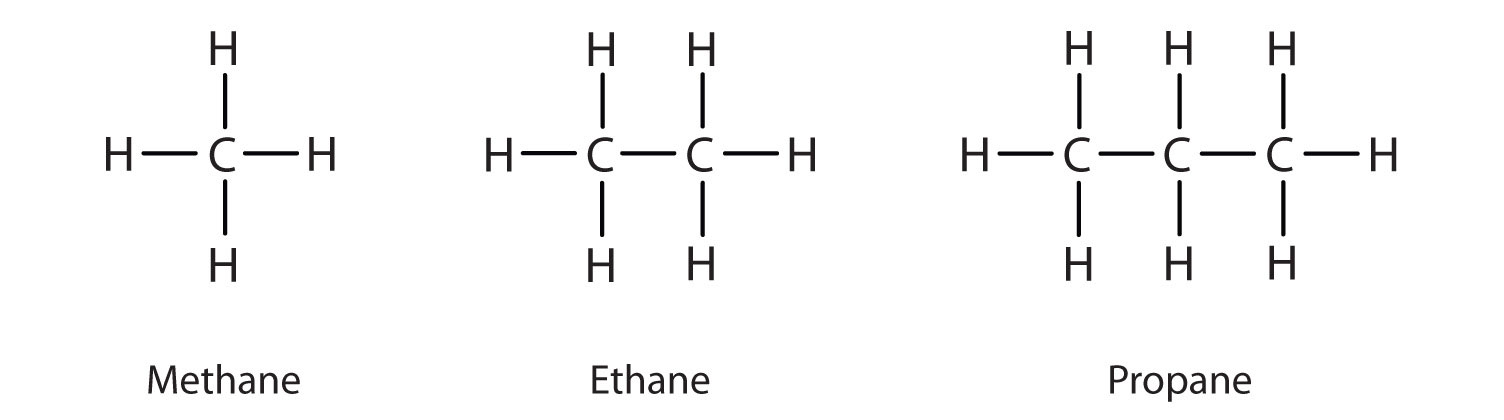
Zobrazená plochá zobrazení nezobrazují přesně vazebné úhly ani geometrii molekul. Methan má tetraedrický tvar, který chemici často znázorňují klíny označujícími vazby vycházející směrem k vám a přerušovanými čarami označujícími vazby, které se od vás vracejí. Obyčejná plná čára označuje vazbu v rovině stránky. Připomeňte si, že teorie VSEPR správně předpovídá tetraedrický tvar molekuly methanu (obrázek \(\PageIndex{2}\)).
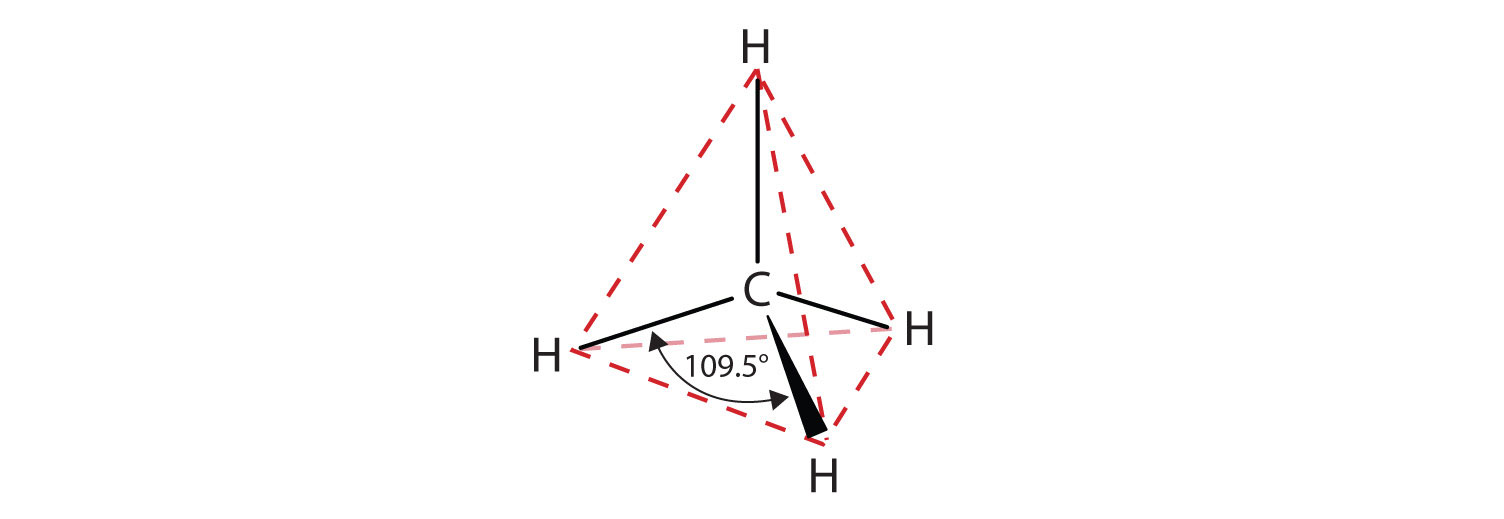
Metan (CH4), etan (C2H6) a propan (C3H8) jsou počátkem řady sloučenin, v níž se libovolné dva členy v posloupnosti liší jedním atomem uhlíku a dvěma atomy vodíku – tedy jednotkou CH2. Prvních deset členů této řady je uvedeno v tabulce \(\PageIndex{1}\).
| Název | Molekulární vzorec (CnH2n + 2) | Kondenzovaný strukturní vzorec | Počet prvků. možných izomerů | |
|---|---|---|---|---|
| methan | CH4 | CH4 | – | |
| ethane | C2H6 | CH3CH3 | – | |
| propan | C3H8 | CH3CH2CH3 | – | |
| butan | C4H10 | CH3CH2CH2CH3 | 2 | |
| pentan | C5H12 | CH3CH2CH2CH3 | 3 | |
| hexan | C6H14 | CH3CH2CH2CH2CH3 | 5 | |
| heptan | C7H16 | CH3CH2CH2CH2CH2CH3 | 9 | |
| oktan | C8H18 | CH3CH2CH2CH2CH2CH2CH3 | CH3CH2CH2CH2CH3 | 18 |
| nonan | C9H20 | CH3CH2CH2CH2CH2CH2CH2CH3 | 35 | |
| dekan | C10H22 | CH3CH2CH2CH2CH2CH2CH2CH2CH3 | 75 |
Považte řadu na obrázku \(\PageIndex{3}\). Posloupnost začíná C3H8 a v každém kroku se přidává jednotka CH2. Každá řada sloučenin, v níž se sousední členy navzájem liší určitým faktorem (zde skupinou CH2), se nazývá homologická řada. Členové takové řady, nazývaní homology, mají vlastnosti, které se liší pravidelným a předvídatelným způsobem. Princip homologie dává organické chemii podobnou organizaci jako periodická tabulka anorganické chemii. Místo nepřehledné řady jednotlivých sloučenin uhlíku můžeme studovat několik členů homologické řady a z nich odvodit některé vlastnosti dalších sloučenin v řadě.
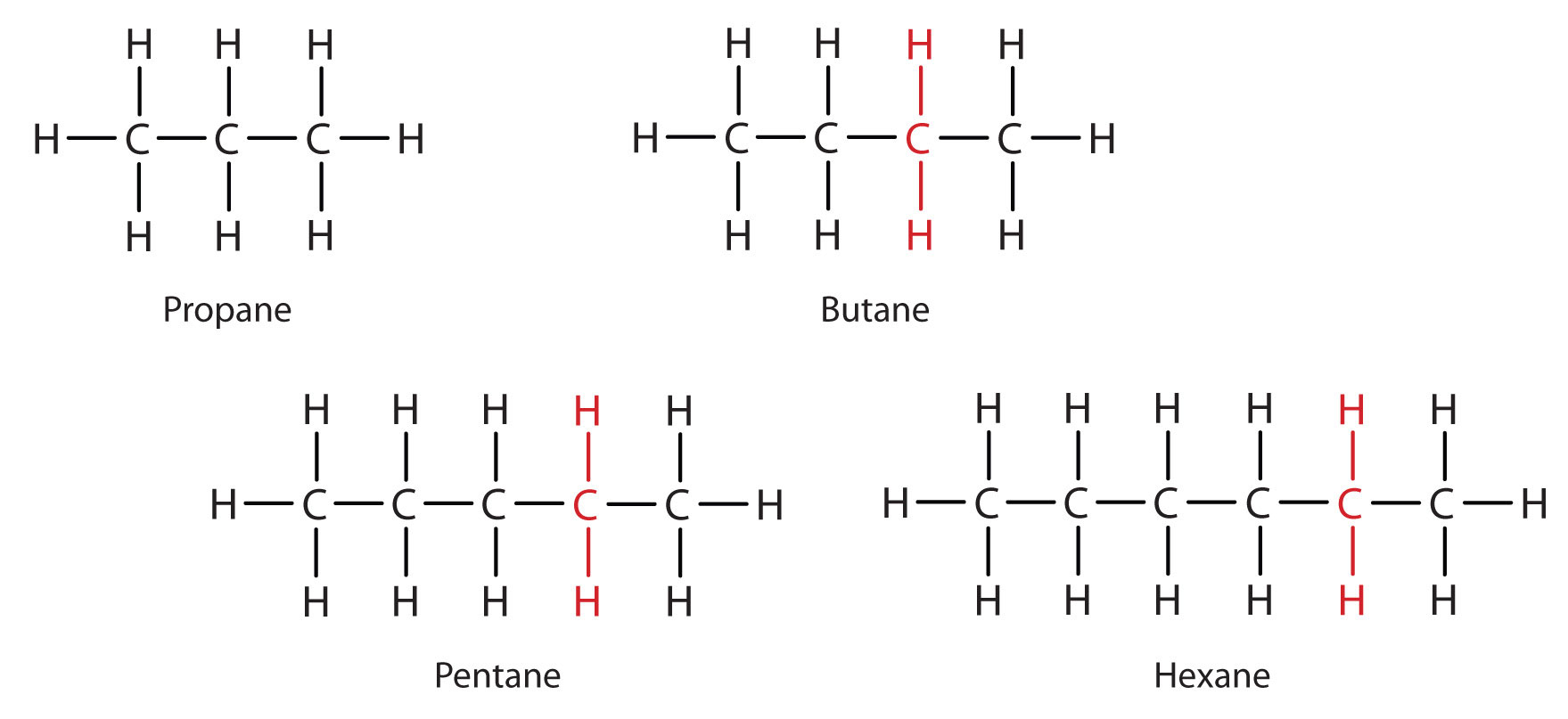
Princip homologie nám umožňuje napsat obecný vzorec pro alkany: CnH2n + 2. Pomocí tohoto vzorce můžeme napsat molekulový vzorec pro libovolný alkan s daným počtem atomů uhlíku. Například alkan s osmi atomy uhlíku má molekulový vzorec C8H(2 × 8) + 2 = C8H18.
Klíčový poznatek
- Prosté alkany existují jako homologická řada, v níž se sousední členy liší jednotkou CH2.
.