Atomii de oxigen au 8 electroni, iar structura învelișului este 2.6.
Configurația electronică a oxigenului neutru gazos în stare fundamentală este .2s2.2p4, iar simbolul termenului este 3P2.
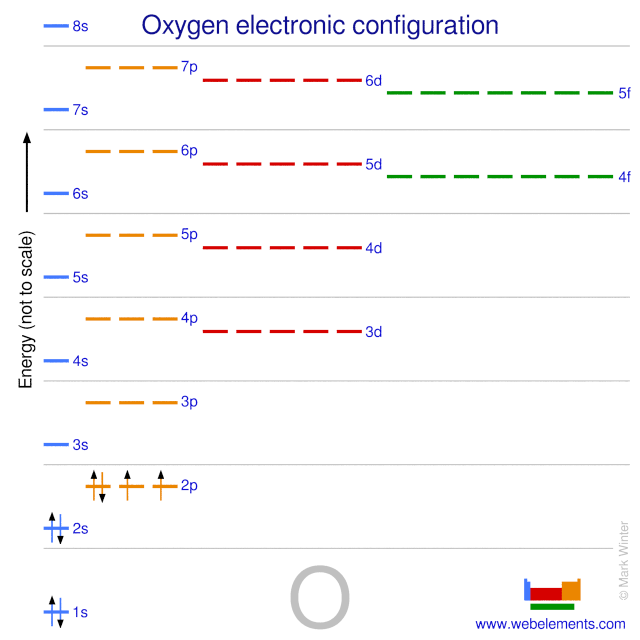
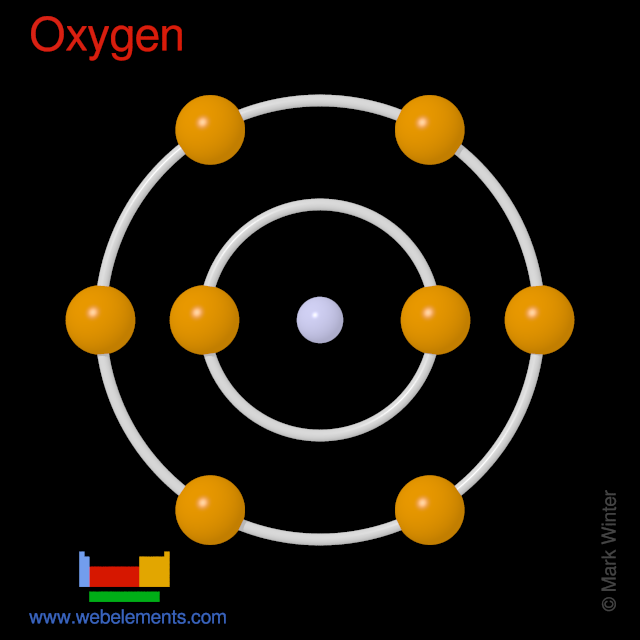
Spectrul atomic
Reprezentare a spectrului atomic al oxigenului.
Energii de ionizare și afinitate electronică
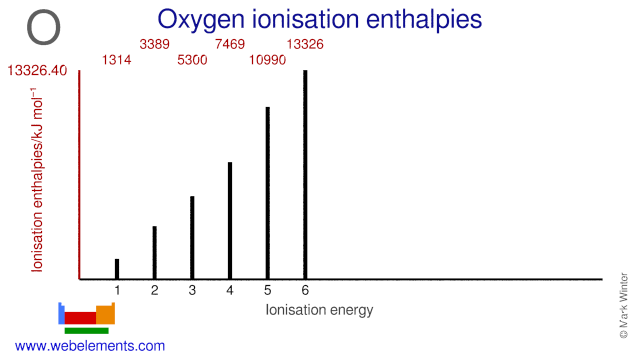
Afinitatea electronică a oxigenului este de 141 kJ mol-1. Energiile de ionizare ale oxigenului sunt date mai jos.
| Numărul energiei de ionizare | Entalpia / kJ mol-1 |
|---|---|
| 1-a | 1313.94 |
| 2-lea | 3388,67 |
| 3-lea | 5300,47 |
| 4-lea | 7469.27 |
| 5-lea | 10989.6 |
| 6-lea | 13326.4 |
| 7-lea | 71334.2 |
| 8-lea | 84078.3 |
Carcini nucleari efectivi
Cele care urmează sunt sarcini nucleare efective „Clementi-Raimondi”, Zeff. Urmați hyperlink-urile pentru mai multe detalii și pentru grafice în diferite formate.
| 1s | 7.6579 | ||||||
|---|---|---|---|---|---|---|---|
| 2s | 4,49 | 2p | 4.45 | ||||
| 3s | (fără date) | 3p | (fără date) | 3d | (fără date) | ||
| 4s | (fără date) | 4p | (fără date) | 4d | (fără date) | 4f | (fără date) |
| 5s | (fără date) | 5p | (fără date) | 5d | (fără date) | ||
| 6s | (fără date) | 6p | (fără date) | ||||
| 7s | |||||||
Aceste sarcini nucleare efective, Zeff, sunt adaptate din următoarele referințe:
- E. Clementi și D.L.Raimondi, J. Chem. Phys. 1963, 38, 2686.
- E. Clementi, D.L.Raimondi, și W.P. Reinhardt, J. Chem. Phys. 1967, 47, 1300.
Energii de legare a electronilor
| Label | Orbital | eV |
|---|---|---|
| K | 1s | 543.1 |
| L I | 2s | 41,6 |
Note
Sunt recunoscător lui Gwyn Williams (Jefferson Laboratory, Virginia, SUA) care a furnizat datele privind energia de legare a electronilor. Datele sunt adaptate din referințele 1-3. Ele sunt tabelate în altă parte pe WWW (referința 4) și în formă de hârtie (referința 5).
- J. A. Bearden și A. F. Burr, „Reevaluation of X-Ray Atomic Energy Levels,” Rev. Mod. Phys. 1967, 39, 125.
- M. Cardona și L. Ley, Eds., Photoemission in Solids I: General Principles (Springer-Verlag, Berlin) cu corecții suplimentare, 1978.
- Gwyn Williams WWW table of values
- D.R. Lide, (Ed.) în Chemical Rubber Company handbook of chemistry and physics, CRC Press, Boca Raton, Florida, SUA, ediția a 81-a, 2000.
- J. C. Fuggle și N. Mårtensson, „Core-Level Binding Energies in Metals,” J. Electron Spectrosc. Relat. Phenom. 1980, 21, 275.
.