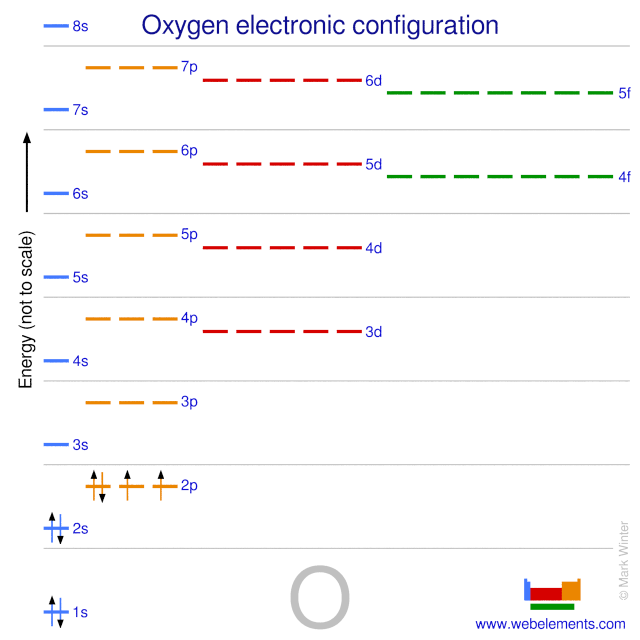
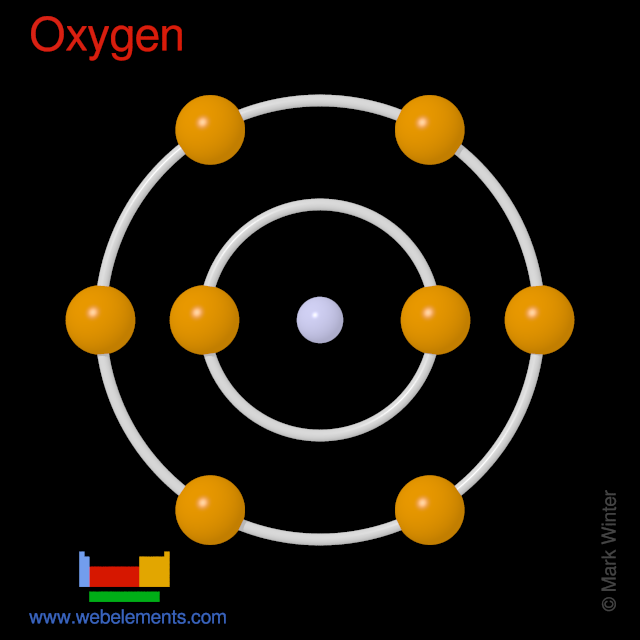
Atomos de oxigénio têm 8 electrões e a estrutura da casca é 2.6.
A configuração electrónica do estado de terra do oxigénio neutro gasoso é .2s2.2p4 e o símbolo do termo é 3P2.
Espectro atómico
Representação do espectro atómico do oxigénio.
Energia de ionização e afinidade dos electrões
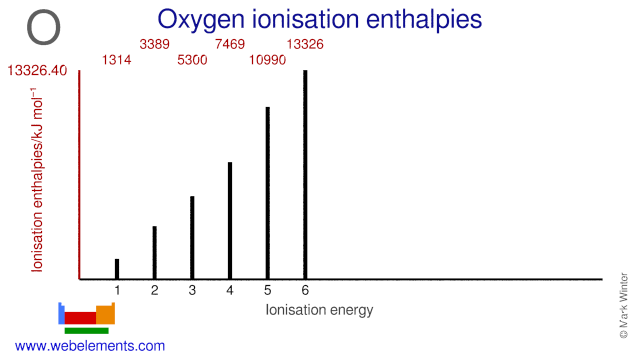
A afinidade dos electrões do oxigénio é de 141 kJ mol-1. As energias de ionização do oxigênio são dadas abaixo.
| Número de energia de ionização | Enthalpy / kJ mol-1 |
|---|---|
| 1st | 131313.94 |
| 2nd | 3388,67> |
| 3rd | 5300,47 |
| 4th | 7469.27 |
| 5º | 10989.6 |
| 6º | 13326.4 |
| 7º | 71334.2 |
| 8º | 84078.3 |
Cargas nucleares efetivas
As seguintes são cargas nucleares efetivas “Clementi-Raimondi”, Zeff. Siga os hyperlinks para mais detalhes e para gráficos em vários formatos.
| 1s | 7.6579 | ||||||
|---|---|---|---|---|---|---|---|
| 2s | 4,49 | 2p | 4.45 | ||||
| 3s | (sem dados) | 3p | (sem dados) | 3d | (sem dados) | ||
| 4s | (sem dados) | 4p | (sem dados) | 4d | (sem dados) | 4f | (sem dados) |
| 5s | (sem dados) | 5p | (sem dados) | 5d | (sem dados) | ||
| 6s | (sem dados) | 6p | (sem dados) | ||||
| 7s | |||||||
Estas cargas nucleares efectivas, Zeff, são adaptadas a partir das seguintes referências:
- E. Clementi e D.L.Raimondi, J. Chem. Phys. 1963, 38, 2686.
- E. Clementi, D.L.Raimondi, e W.P. Reinhardt, J. Chem. Phys. 1967, 47, 1300.
Energia de ligação ao electrão
| Label | Orbital | eV |
|---|---|---|
| K | 1s | 543.1 |
| L I | 2s | 41.6 |
Notas
Sou grato a Gwyn Williams (Jefferson Laboratory, Virginia, EUA) que forneceu os dados de energia de ligação de electrões. Os dados são adaptados a partir das referências 1-3. Eles são tabulados em outro lugar na WWW (referência 4) e em papel (referência 5).
- J. A. Bearden e A. F. Burr, “Reevaluation of X-Ray Atomic Energy Levels”, Rev. Mod. Phys., 1967, 39, 125.
- M. Cardona e L. Ley, Eds., Photoemission in Solids I: General Principles (Springer-Verlag, Berlin) with additional corrections, 1978.
- Gwyn Williams WWW table of values
- D.R. Lide, (Ed.) in Chemical Rubber Company handbook of chemistry and physics, CRC Press, Boca Raton, Florida, USA, 81st edition, 2000.
- J. C. Fuggle e N. Mårtensson, “Core-Level Binding Energies in Metals”, J. Electron Spectrosc. Relat. Phenom., 1980, 21, 275.